Exetat Sciences 2025_Scientifique
Question 1
1. Un échantillon de NaI est injecté à un patient dans le cadre du traitement d’un cancer de la thyroïde. Si l’échantillon a une radioactivité de 10,000 dés/min à 8h50’, sachant que sa période radioactive ou demi-vie est de 25 minutes. Sa radioactivité (en dés/min) à 10h05’ sera :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 1,250 dés/min (proposition c).
Explication :
La période radioactive (demi-vie) est de 25 minutes.
On passe de 8h50’ à 10h05’, soit 1h15’ = 75 minutes.
Le nombre de périodes écoulées est :
\[
n = \frac{75}{25} = 3
\]
La loi de décroissance radioactive est :
\[
A = A_0 \left(\frac{1}{2}\right)^n
\]
où \( A_0 = 10,000 \) dés/min et \( n = 3 \).
Donc :
\[
A = 10,000 \left(\frac{1}{2}\right)^3
= 10,000 \times \frac{1}{8}
= 1,250 \ \text{dés/min}
\]
La radioactivité à 10h05’ est donc :
\[
\boxed{1,250 \ \text{dés/min}}
\]
2. Pendant le tour de salles dans un centre de santé, le médecin prescrit pour un octogénaire \(2 \times 10^{21}\) molécules de l’acide acétylsalicylique ou aspirine \(\text{C}_9\text{H}_8\text{O}_4\). La masse de ce médicament (en mg) est :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 600 mg (proposition b).
Explication :
On calcule d’abord la masse molaire de l’aspirine \(\text{C}_9\text{H}_8\text{O}_4\) :
\[
M = 9 \times 12 + 8 \times 1 + 4 \times 16 = 108 + 8 + 64 = 180 \ \text{g/mol}
\]
On utilise le nombre d’Avogadro :
\[
N_A = 6{,}02 \times 10^{23} \ \text{molécules/mol}
\]
La quantité de matière correspondant à \(2 \times 10^{21}\) molécules est :
\[
n = \frac{2 \times 10^{21}}{6{,}02 \times 10^{23}} \approx 3{,}32 \times 10^{-3} \ \text{mol}
\]
La masse correspondante est :
\[
m = n \times M \approx 3{,}32 \times 10^{-3} \times 180 \approx 0{,}598 \ \text{g}
\]
En milligrammes :
\[
0{,}598 \ \text{g} \approx 598 \ \text{mg} \approx 600 \ \text{mg}
\]
Donc la masse du médicament est :
\[
\boxed{600 \ \text{mg}}
\]
3. Dans un laboratoire d’une usine de fabrication des médicaments, il est demandé de diluer deux fois une solution molaire obtenue par dissolution de 52,8 g d’acide ascorbique (ou vitamine C), de formule ci‑contre. Le volume (en litre) de la solution diluée vaut : 
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32
Réponse correcte : 0,6 L (proposition c).
Explication :
La formule brute de l’acide ascorbique (vitamine C) est \(\text{C}_6\text{H}_8\text{O}_6\).
Sa masse molaire est :
\[
M = 6 \times 12 + 8 \times 1 + 6 \times 16 = 72 + 8 + 96 = 176 \ \text{g/mol}
\]
La quantité de matière dans 52,8 g est :
\[
n = \frac{52,8}{176} = 0,3 \ \text{mol}
\]
La solution est dite « molaire », donc sa concentration est :
\[
C = 1 \ \text{mol/L}
\]
Le volume de la solution initiale est alors :
\[
V\_{\text{initial}} = \frac{n}{C} = \frac{0,3}{1} = 0,3 \ \text{L}
\]
Diluer deux fois signifie doubler le volume (dilution au facteur 2) :
\[
V\_{\text{final}} = 2 \times V\_{\text{initial}} = 2 \times 0,3 = 0,6 \ \text{L}
\]
Donc le volume de la solution diluée est :
\[
\boxed{0,6 \ \text{L}}
\]
4. Voici ci‑contre le schéma de l’électrolyse de l’eau pour produire principalement de l’hydrogène gazeux.
Le chiffre 3 désigne :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32
Réponse correcte : L’oxygène à recueillir (proposition b).
Explication :
Dans l’électrolyse de l’eau :
- Au niveau de la cathode (borne négative), on forme du dihydrogène \(H_2\).
- Au niveau de l’anode (borne positive), on forme du dioxygène \(O_2\).
Sur le schéma, le chiffre 3 pointe vers le tube du côté de l’anode, où se dégage le dioxygène.
Ainsi, le chiffre 3 désigne :
\[
\boxed{\text{l’oxygène à recueillir}}
\]
5. En vue d’une analyse au laboratoire, un chimiste pèse 2,2 g de soude caustique. Il ajoute de l’eau distillée et une goutte d’un indicateur coloré. La neutralisation s’obtient par adjonction de 60 ml d’une solution de l’acide sulfurique 0,3 M. Le pourcentage NaOH contenu dans cette solution est :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 65,4 % (proposition d).
Explication :
L’équation de neutralisation est :
\[
2 \text{NaOH} + \text{H}_2\text{SO}_4 \rightarrow \text{Na}_2\text{SO}_4 + 2 \text{H}_2\text{O}
\]
On calcule la quantité de matière d’acide sulfurique :
\[
n(\text{H}_2\text{SO}_4) = C \times V = 0,3 \times 0,060 = 0,018 \ \text{mol}
\]
D’après la stœchiométrie, il faut 2 moles de NaOH pour 1 mole de H2SO4 :
\[
n(\text{NaOH}) = 2 \times 0,018 = 0,036 \ \text{mol}
\]
Masse molaire de NaOH :
\[
M(\text{NaOH}) = 40 \ \text{g/mol}
\]
Masse de NaOH pur dans l’échantillon :
\[
m(\text{NaOH}) = 0,036 \times 40 = 1,44 \ \text{g}
\]
Pourcentage massique de NaOH dans les 2,2 g de soude caustique :
\[
\% \text{NaOH} = \frac{1,44}{2,2} \times 100 \approx 65,4 \ \%
\]
Donc le pourcentage de NaOH est :
\[
\boxed{65,4 \ \%}
\]
6. Lors de la réaction d’oxydo‑réduction, l’acide sulfurique concentré et chaud est un agent oxydant vis‑à‑vis du mercure. On obtient des ions mercuriques et un dégagement de dioxyde de soufre. La masse de mercure à utiliser pour obtenir 3 litres de dioxyde de soufre gazeux dans les conditions normales vaut :
Réaction chimique : \(\text{Hg} + \text{H}_2\text{SO}_4 \rightarrow \text{HgSO}_4 + \text{SO}_2 + \text{H}_2\text{O}\).
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 26,86 g (proposition b).
Explication :
Dans l’équation donnée, il y a proportion stœchiométrique :
\[
\text{Hg} \longrightarrow \text{SO}_2
\]
Donc 1 mole de Hg produit 1 mole de SO2.
À conditions normales, le volume molaire d’un gaz est :
\[
V_m = 22,4 \ \text{L/mol}
\]
La quantité de matière de SO2 correspondant à 3 L est :
\[
n(\text{SO}_2) = \frac{3}{22,4} \approx 0,134 \ \text{mol}
\]
Par stœchiométrie :
\[
n(\text{Hg}) = n(\text{SO}_2) \approx 0,134 \ \text{mol}
\]
La masse molaire du mercure est :
\[
M(\text{Hg}) = 200,59 \ \text{g/mol}
\]
La masse de Hg nécessaire est donc :
\[
m(\text{Hg}) = n \times M \approx 0,134 \times 200,59 \approx 26,86 \ \text{g}
\]
Donc la masse de mercure requise est :
\[
\boxed{26,86 \ \text{g}}
\]
7. Pendant la sèche d’eau, Jeanne va à la rivière puiser de l’eau, elle soulève un seau de 3 kg à une hauteur de 1 mètre. (prendre g = 9,8 m/s²)
Le travail effectué pour soulever le seau d’eau vaut :
Réponse Correcte : c. 29,43 J
Explication :
Le travail \( W \) d'une force nécessaire pour soulever un corps est équivalent à l'énergie potentielle de pesanteur acquise par ce corps.
1. Données du problème :
* Masse (m) = 3 kg
* Hauteur (h) = 1 m
* Accélération de la pesanteur (g) = 9,8 m/s²
2. Formule mathématique :
Le travail est calculé par la relation :
\[ W = m \cdot g \cdot h \]
3. Application numérique :
\[ W = 3 \cdot 9,8 \cdot 1 \]
\[ W = 29,4 \text{ Joules} \]
Note : La valeur de 29,43 J dans l'assertion c correspond à l'utilisation d'une valeur de \( g \) légèrement plus précise (\( 9,81 \text{ m/s}^2 \)) lors de la conception de l'examen, mais 29,4 J en est la valeur arrondie directe.
8. Une mangue de masse 10 g tombe à 120,5 m du sol. Si g = 9,8 m/s² et si les frottements sont supposés négligeables.
L’énergie cinétique de la mangue en arrivant au sol sera de :
Réponse Correcte : c. 11,809 J
Explication :
Selon le principe de conservation de l'énergie mécanique, en l'absence de frottements, l'énergie potentielle initiale (Eₚ) de la mangue au sommet est intégralement convertie en énergie cinétique (Eₖ) au moment où elle touche le sol.
1. Données du problème :
* Masse (m) = 10 g = 0,01 kg
* Hauteur (h) = 120,5 m
* Accélération de la pesanteur (g) = 9,8 m/s²
2. Formule mathématique :
L'énergie cinétique finale est égale à l'énergie potentielle initiale :
\[ E_k = E_p = m \cdot g \cdot h \]
3. Application numérique :
\[ E_k = 0,01 \cdot 9,8 \cdot 120,5 \]
\[ E_k = 0,098 \cdot 120,5 \]
\[ E_k = 11,809 \text{ Joules} \]
La valeur obtenue est de 11,809 J, ce qui correspond exactement à l'assertion c.
9. La R.D.C organise un jeu concours des cyclistes, un des cyclistes commence avec une accélération de 6 m/s². Après un certain temps, la voie devient dégagée, il accélère et son accélération devient 26 m/s².
L’accélération moyenne de ce mobile dans ce trajet vaut (en m/s²) :
Réponse Correcte : b. 16
Explication :
L'accélération moyenne (\( a_{moy} \)) d'un mobile subissant deux accélérations constantes successives sur un même trajet est définie par la moyenne arithmétique de ces accélérations.
1. Données du problème :
* Première accélération (\( a_1 \)) = 6 m/s²
* Deuxième accélération (\( a_2 \)) = 26 m/s²
2. Formule mathématique :
L'accélération moyenne est donnée par la relation :
\[ a_{moy} = \frac{a_1 + a_2}{2} \]
3. Application numérique :
\[ a_{moy} = \frac{6 + 26}{2} \]
\[ a_{moy} = \frac{32}{2} \]
\[ a_{moy} = 16 \text{ m/s}^2 \]
Le résultat est de 16 m/s², ce qui correspond à l'assertion b.
10. L’équipe nationale de basketball joue dans un terrain. Un des joueurs lance une balle verticalement vers le haut avec une vitesse de 30 m/s.
Si g = 10 m/s², la balle retombera dans les mains de ce joueur après :
Réponse Correcte : c. 6s
Explication :
Ce problème porte sur le mouvement rectiligne uniformément varié (MRUV) sous l'effet de la pesanteur. On cherche le temps total de vol (\( t_{total} \)).
1. Données du problème :
* Vitesse initiale (\( v_0 \)) = 30 m/s
* Accélération de la pesanteur (g) = 10 m/s²
2. Calcul du temps de montée (\( t_m \)) :
À la hauteur maximale, la vitesse finale est nulle (\( v = 0 \)).
Selon la formule : \( v = v_0 - g \cdot t_m \)
\[ 0 = 30 - 10 \cdot t_m \]
\[ 10 \cdot t_m = 30 \]
\[ t_m = \frac{30}{10} = 3 \text{ s} \]
3. Calcul du temps total (\( t_{total} \)) :
Dans un lancer vertical sans frottement, le temps de montée est égal au temps de descente. Par conséquent, le temps nécessaire pour que la balle retombe dans les mains du joueur est :
\[ t_{total} = 2 \cdot t_m \]
\[ t_{total} = 2 \cdot 3 \text{ s} = 6 \text{ s} \]
Le temps total est donc de 6 s, ce qui correspond à l'assertion c.
11. Dans un atelier de menuiserie, un menuisier utilise un marteau de 3 kg pour faire pénétrer un clou dans une planche. Ce marteau aborde la tête de ce clou à la vitesse de 4 m/s. La force à exercer pour que le clou pénètre dans la planche à 1 cm vaut :
Réponse Correcte : d. 2.400 N
Explication :
Pour résoudre ce problème, nous utilisons le théorème de l'énergie cinétique. Le travail de la force de résistance (\( W \)) opposée par la planche est égal à la variation de l'énergie cinétique (\( \Delta E_k \)) du marteau jusqu'à son arrêt complet.
1. Données du problème :
* Masse (m) = 3 kg
* Vitesse initiale (\( v \)) = 4 m/s
* Distance de pénétration (d) = 1 cm = 0,01 m
* Vitesse finale = 0 m/s (arrêt)
2. Formule de l'énergie cinétique initiale :
\[ E_k = \frac{1}{2} \cdot m \cdot v^2 \]
\[ E_k = \frac{1}{2} \cdot 3 \cdot 4^2 = \frac{1}{2} \cdot 3 \cdot 16 = 24 \text{ Joules} \]
3. Relation entre travail et force :
Le travail effectué par la force (\( F \)) sur la distance (\( d \)) est :
\[ W = F \cdot d \]
D'après le théorème de l'énergie cinétique : \( W = E_k \).
4. Calcul de la force :
\[ F = \frac{E_k}{d} \]
\[ F = \frac{24}{0,01} \]
\[ F = 2.400 \text{ N} \]
La force à exercer est donc de 2.400 N, ce qui correspond à l'assertion d.
12. Dans les conditions bien précises de l'étude d'un pendule simple \(\pi^{2} = 10\) et \(g = 10\ m/s^{2}\). Pour obtenir une période de 6 secondes, il faut une longueur de :
Réponse Correcte : c. 9 m
Explication :
La période \(T\) d'un pendule simple dépend de sa longueur \(l\) et de l'accélération de la pesanteur \(g\).
1. Données du problème :
* Période (\(T\)) = 6 s
* Accélération de la pesanteur (\(g\)) = 10 m/s²
* Constante (\(\pi^{2}\)) = 10
2. Formule de la période d'un pendule simple :
\[ T = 2\pi \sqrt{\frac{l}{g}} \]
3. Transformation pour isoler la longueur (\(l\)) :
Élevons la formule au carré :
\[ T^{2} = 4\pi^{2} \frac{l}{g} \]
D'où :
\[ l = \frac{T^{2} \cdot g}{4\pi^{2}} \]
4. Application numérique :
En remplaçant par les valeurs données :
\[ l = \frac{6^{2} \cdot 10}{4 \cdot 10} \]
\[ l = \frac{36 \cdot 10}{40} \]
\[ l = \frac{36}{4} \]
\[ l = 9\ \text{m} \]
La longueur nécessaire est donc de 9 m, ce qui correspond à l'assertion c.
13. Monsieur MUSIKE, professeur des sciences à KITONA s’apprête à mettre en place un robot capable de résoudre une équation du 2ème degré à 2 inconnus dans R. Les apprenants de la 4ème année des humanités sciences de l’école voisine sont appelés pour produire la démarche pour la réalisation de chaque tâche.
Identifiez le symbole de début et de fin d’un processus. 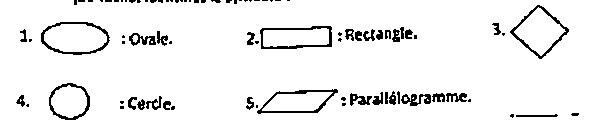
Réponse Correcte : 1. Ovale.
Explication :
Dans la représentation graphique d'un algorithme (appelée organigramme ou ordonnançage), chaque forme géométrique possède une signification conventionnelle précise pour décrire les étapes d'un processus informatique.
* L'Ovale (1) : Il est utilisé comme "terminal" pour marquer exclusivement le DEBUT et la FIN d'un algorithme ou d'un processus.
* Le Parallélogramme (5) : Il sert à représenter les opérations d'Entrée (lecture de données) ou de Sortie (affichage des résultats).
* Le Rectangle (2) : Il symbolise un traitement ou une instruction (calcul, affectation).
* Le Losange (3) : Il représente une condition ou un test (prise de décision "Si... Alors").
Puisque la question demande d'identifier le symbole de début et de fin, il s'agit de l'ovale.
14. Identifiez l’équipement d’interconnexion des réseaux qui permet de relier que 2 réseaux locaux homogènes.
Réponse Correcte : d. Ponts (Bridges).
Explication :
L'interconnexion de réseaux nécessite des équipements spécifiques selon la nature des réseaux à relier (homogènes ou hétérogènes) et la couche du modèle OSI concernée.
1. Définition du Pont (Bridge) :
Le pont est un dispositif matériel qui fonctionne au niveau de la couche liaison de données (couche 2 du modèle OSI). Son rôle principal est de segmenter un réseau ou de relier deux réseaux locaux (LAN) qui utilisent le même protocole (réseaux homogènes).
2. Pourquoi cette réponse ? :
* Le Pont (d) : Il est conçu pour connecter deux réseaux locaux de même type (homogènes) en filtrant les trames basées sur les adresses MAC.
* La Passerelle (b) : Elle relie des réseaux hétérogènes (architectures ou protocoles différents).
* Le Routeur (c) : Il relie plusieurs réseaux (homogènes ou non) en déterminant le meilleur chemin pour les paquets de données (couche 3).
* Le Répéteur (e) : Il se contente de régénérer le signal électrique pour augmenter la distance du réseau, sans distinguer les réseaux.
Conclusion : Pour relier spécifiquement deux réseaux locaux homogènes, l'équipement approprié est le Pont (Bridge), ce qui correspond à l'assertion d.
15. Indiquez la proposition qui associe correctement chaque type de réseau (I) à sa situation appropriée (II).
I.
a. Réseau local LAN
b. Réseau étendu WAN
c. Réseau local MAN
d. Aucun réseau.
II.
1. Un équipement qui ne se connecte pas directement à la ligne de transmission.
2. Des apprenants d’une même ville veulent s’échanger des informations.
3. Un préfet de l’école doit informer les enseignants d’une même initiative.
4. Vingt enseignants aux quatre coins de la R.D.C veulent partager leurs expériences.
5. Un enseignant veut imprimer les corrigés sur son imprimante personnelle.
Réponse Correcte : 1. a5 ; b4 ; c2 ; d1.
Explication :
Pour résoudre cette question, il faut faire correspondre la portée géographique de chaque type de réseau à la situation décrite :
1. Analyse des correspondances :
* a -> 5 : Le réseau LAN (Local Area Network) couvre une zone géographique restreinte (une pièce, une maison). Un enseignant imprimant sur son imprimante personnelle utilise un réseau local (ou un lien direct assimilé au local).
* b -> 4 : Le réseau WAN (Wide Area Network) couvre de très grandes distances. Vingt enseignants situés aux quatre coins de la R.D.C. (un pays entier) nécessitent un WAN pour communiquer.
* c -> 2 : Le réseau MAN (Metropolitan Area Network) interconnecte des utilisateurs à l'échelle d'une ville. Des apprenants d'une même ville correspondent donc au MAN.
* d -> 1 : "Aucun réseau" correspond logiquement à un équipement qui n'est pas connecté à une ligne de transmission.
2. Vérification de la proposition :
En regroupant ces couples, nous obtenons : a5, b4, c2, d1. Cette combinaison correspond exactement à la proposition 1 du bloc III.
Conclusion : La proposition (III) correcte est la 1.
