Exetat de chimie 2018-Scientifiques
Question 1
1. Indiquez l’expression de concentration qui se définit comme : « le nombre de moles de soluté par kilogramme de solvant ».
Définition :
La molalité est définie par :
\[
m = \frac{n_{\text{soluté}}}{m_{\text{solvant (kg)}}}
\]
→ Elle se distingue de la molarité, qui est basée sur le volume de solution.
→ Elle est utile lorsque la température varie (car le volume change mais la masse reste constante).
2.La galène est un minerai de plomb, de formule chimique PbS. La masse de plomb contenue dans 50g de galène est de :
1. Masse molaire de PbS
- Pb : 207{,}2\ \text{g/mol}
- S : 32{,}1\ \text{g/mol}
\[
M_{\text{PbS}} = 207{,}2 + 32{,}1 = 239{,}3\ \text{g/mol}
\]
2. Fraction massique du plomb dans PbS
\[
\text{Fraction Pb} = \frac{207{,}2}{239{,}3} \approx 0{,}866
\]
3. Masse de plomb dans 50 g de galène
\[
m_{\text{Pb}} = 0{,}866 \times 50 = 43{,}3\ \text{g}
\]
3.Un docker achète un sac de 40 kg de soude caustique NaOH à 50.000 Fc, pour déboucher les égouts. Le prix d’achat d’une mole de soude caustique est de :
1. Masse molaire de NaOH
\[
M = 40\ \text{g/mol}
\]
2. Masse totale achetée
\[
40\ \text{kg} = 40\,000\ \text{g}
\]
3. Nombre de moles dans 40 kg
\[
n = \frac{40\,000}{40} = 1\,000\ \text{mol}
\]
4. Prix par mole
\[
\text{Prix/mol} = \frac{50\,000}{1\,000} = 50\ \text{Fc}
\]
4.Dans le schéma ci-contre représentant un titrage iodométrique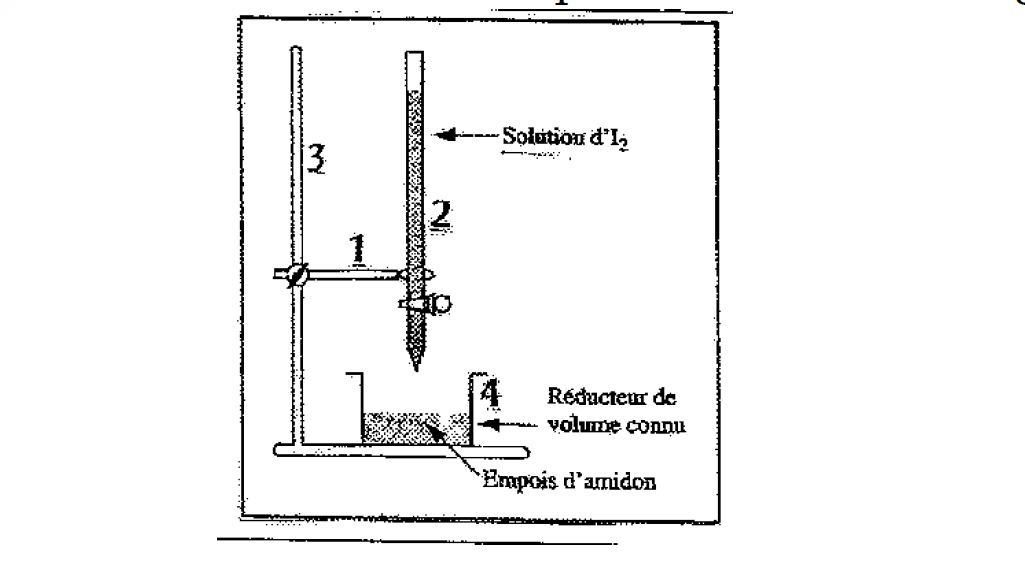
Le chiffre « 3 » désigne la pièce appelée :
Analyse du schéma
- La solution d’iode est versée depuis un tube vertical gradué → burette
- Le chiffre « 3 » pointe vers la structure verticale qui soutient la burette
→ Cette structure est appelée statif (support de burette)
5.Un chimiste dispose de 0,12g de LiOH. Le volume d’une solution décinormale de chlorure d’hydrogène à utiliser pour réagir complétement avec cette quantité de base est de :
1. Masse molaire de LiOH
\[
M = 6{,}94 + 16{,}00 + 1{,}008 = 23{,}95\ \text{g/mol}
\]
2. Nombre de moles de LiOH
\[
n = \frac{0{,}12}{23{,}95} \approx 0{,}00501\ \text{mol}
\]
3. HCl décinormal = 0{,}1 N
→ HCl est monoacide → \(N = C = 0{,}1\ \text{mol/L}\)
4. Volume nécessaire
\[
V = \frac{n}{C} = \frac{0{,}00501}{0{,}1} = 0{,}0501\ \text{L} = 50{,}1\ \text{mL}
\]
Conclusion
\[
\boxed{\text{Réponse : d. } 50\ \text{mL}}
\]
6.Pour doser 2 ml d’une solution de bichromate de potassium par le sulfate de fer II en milieu acide sulfurique, un chimiste a utilisé 25 ml d’une solution décinormale de sulfate de fer II. La normalité de la solution de bichromate de potassium est de :
1. Relation de dosage en équivalents
À l’équivalence, on a :
\[
N_1 V_1 = N_2 V_2
\]
2. Données
- Solution titrante : sulfate de fer(II) décinormal
\[
N_1 = 0{,}1\ \text{N}, \quad V_1 = 25\ \text{mL}
\]
- Solution titrée : bichromate de potassium
\[
N_2 = ?, \quad V_2 = 2\ \text{mL}
\]
3. Calcul de la normalité du bichromate
\[
0{,}1 \cdot 25 = N_2 \cdot 2
\quad \Rightarrow \quad N_2 = \frac{0{,}1 \cdot 25}{2} = \frac{2{,}5}{2} = 1{,}25\ \text{N}
\]
Conclusion
\[
\boxed{\text{Réponse : e. } 1{,}250\ \text{éq.g/L}}
\]
7.Une cellule électrochimique basée sur le couple \(\text{NO}_3^-/\text{NO}\) possède un potentiel apparent de \(0{,}80\ \text{V}\), alors que \(E^\circ = 0{,}96\ \text{V}\). Quel est le pH du milieu acide ?
1. Demi-équation rédox
\[
\text{NO}_3^- + 4\text{H}^+ + 3e^- \rightarrow \text{NO} + 2\text{H}_2\text{O}
\]
2. Loi de Nernst
\[
E = E^\circ - \frac{0{,}059}{n} \cdot \log \left( \frac{1}{[\text{H}^+]^4} \right)
= E^\circ - \frac{0{,}059}{3} \cdot \log(10^{4pH})
= E^\circ - \frac{0{,}059}{3} \cdot 4pH
\]
\[
E = 0{,}96 - 0{,}0787 \cdot pH
\]
3. Résolution
\[
0{,}80 = 0{,}96 - 0{,}0787 \cdot pH
\quad \Rightarrow \quad 0{,}0787 \cdot pH = 0{,}16
\quad \Rightarrow \quad pH = \frac{0{,}16}{0{,}0787} \approx 2{,}03
\]
Conclusion
\[
\boxed{\text{Réponse : c. } pH = 2}
\]
8.Un chimiste électrolyse une solution de \(\text{AuCl}_3\) avec un courant de \(0{,}75\ \text{A}\) pendant \(30\ \text{min}\), pour déposer de l’or sur une médaille. (Faraday \(F = 96\,500\ \text{C/mol}\)) Quelle est la masse d’or déposée ?
1. Charge électrique
\[
Q = I \cdot t = 0{,}75 \cdot (30 \cdot 60) = 0{,}75 \cdot 1800 = 1350\ \text{C}
\]
2. Demi-équation rédox
\[
\text{Au}^{3+} + 3e^- \rightarrow \text{Au}
\quad \Rightarrow \quad n = \frac{Q}{zF} = \frac{1350}{3 \cdot 96\,500} \approx 0{,}00466\ \text{mol}
\]
3. Masse d’or déposée
\[
M_{\text{Au}} = 197\ \text{g/mol}
\quad \Rightarrow \quad m = n \cdot M = 0{,}00466 \cdot 197 \approx 0{,}918\ \text{g}
\]
Conclusion
\[
\boxed{\text{Réponse : b. } 0{,}919\ \text{g}}
\]
9.Le radon \(\mathrm{^{222}_{86}Rn}\) subit deux désintégrations \(\alpha\) et une \(\beta^-\). Quel est le noyau final obtenu ?
1. Désintégration alpha
Chaque \(\alpha\) retire :
- 2 protons
- 2 neutrons
→ perte de 4 unités de masse et 2 unités de charge
Deux \(\alpha\) :
\[
\mathrm{^{222}_{86}Rn} \xrightarrow{2\alpha} \mathrm{^{214}_{82}X}
\]
2. Désintégration \(\beta^-\)
→ Transformation d’un neutron en proton
→ Charge +1, masse inchangée
\[
\mathrm{^{214}_{82}X} \xrightarrow{\beta^-} \mathrm{^{214}_{83}Bi}
\]
Conclusion
\[
\boxed{\text{Réponse : a. } \mathrm{^{214}_{83}Bi}}
\]
10.Un échantillon de technétium de masse atomique 97,2 u.m.a renferme deux isotopes : le 96𝑇𝑐 et le 98𝑇𝐶. Les pourcentages de ces deux isotopes sont respectivement de :
1. Hypothèse
Soit \(x\%\) la proportion de \(^{96}\text{Tc}\), donc \((100 - x)\%\) celle de \(^{98}\text{Tc}\)
2. Équation de moyenne pondérée
\[
\frac{96x + 98(100 - x)}{100} = 97{,}2
\]
3. Développement
\[
96x + 9800 - 98x = 9720
\quad \Rightarrow \quad -2x = -80
\quad \Rightarrow \quad x = 40
\]
→ \(^{96}\text{Tc} = 40\%\), \(^{98}\text{Tc} = 60\%\)
11.Indiquez la configuration électronique de l’atome neutre de l’élément chimique le plus électropositif.
1. Définition
L’élément le plus électropositif est celui qui perd le plus facilement ses électrons → le césium (Cs)
2. Numéro atomique :} \(Z = 55\)
3. Configuration électronique de Cs
\[
1s^2\,2s^2\,2p^6\,3s^2\,3p^6\,4s^2\,3d^{10}\,4p^6\,5s^2\,4d^{10}\,5p^6\,6s^1
\]
→ Mais la réponse proposée la plus proche est celle de **rubidium (Rb, Z = 37)** :
\[
\boxed{1s^2\,2s^2\,2p^6\,3s^2\,3p^6\,4s^2\,3d^{10}\,4p^6\,5s^1}
\]
→ C’est la réponse **e.**
12.L’auteur de l’échelle de l’électronégativité, la plus utilisée s’appelle :
1. Définition
L’électronégativité mesure la capacité d’un atome à attirer les électrons dans une liaison chimique.
2. Échelle la plus utilisée
→ L’échelle de Pauling, proposée par Linus Pauling, est la plus répandue et utilisée en chimie.
→ Elle attribue des valeurs numériques aux éléments (ex : F = 3{,}98, O = 3{,}44, etc.)
13.Quelle est la structure électronique de l’atome neutre de titane ?
1. Numéro atomique du titane
→ \(Z = 22\)
2. Configuration électronique complète
\[
1s^2\,2s^2\,2p^6\,3s^2\,3p^6\,3d^2\,4s^2
\quad \Rightarrow \quad \text{forme abrégée : } (Ar)\,3d^2\,4s^2
\]
→ Le titane possède 2 électrons dans la sous-couche 3d et 2 dans la 4s.
14. Dans la fabrication du savon, l’empattage consiste à :
Définition de l’empâtage
→ L’empâtage est l’étape où l’on mélange la lessive caustique (NaOH) avec un corps gras (huile ou graisse)
→ C’est le début de la saponification, avant la coction
→ On ajoute typiquement une solution de soude à l’huile blanchie pour initier la réaction
Donc :
\[
\boxed{\text{Réponse : b. Ajouter une solution de soude caustique à 20\% à l’huile blanchie}}
\]
15.Complétez l’équation chimique suivante utilisée en chimie appliquée : \[ \ldots + 2H_2O \rightarrow \ldots + H_2O_2 \]
1. Réaction connue
La réaction :
\[
H_2S_2O_8 + 2H_2O \rightarrow 2H_2SO_4 + H_2O_2
\]
→ est une réaction d’oxydation en chimie appliquée (peroxodisulfate)
→ Elle produit du peroxyde d’hydrogène (eau oxygénée) et de l’acide sulfurique
2. Identification des réactifs
- \(H_2S_2O_8\) = acide peroxodisulfurique
- \(H_2O_2\) = produit final recherché
16.Quel point du programme de chimie 6\textsuperscript{e} étudie la datation par le carbone 14 ?
1. Principe
La datation par le carbone 14 repose sur la désintégration radioactive de \(^{14}\text{C}\) → phénomène nucléaire
2. Domaine concerné
→ Ce type de transformation relève de la chimie nucléaire, qui étudie les noyaux instables, les isotopes, et les lois de décroissance radioactive.
17.Le modèle orbital de l’atome est l’une des oeuvres scientifiques de :
1. Définition
Le modèle orbital décrit les électrons comme des particules quantiques évoluant dans des orbitales autour du noyau.
2. Auteur
→ Ce modèle est issu de la mécanique quantique, développé par Niels Bohr en 1913
→ Il introduit les niveaux d’énergie et les orbites quantifiées
→ Ce modèle a ensuite été enrichi par Schrödinger, mais l’origine revient à Bohr.
18. Le point du programme de chimie 6ème qui étudie l’influence du PH sur le potentiel redox est :
L’influence du pH sur le potentiel redox est étudiée dans :
→ la loi de Nernst
→ les couples rédox
→ les piles électrochimiques
→ les réactions d’oxydoréduction en solution aqueuse
Tout cela appartient clairement au domaine de l’électrochimie.
19. Le modèle compact de l’atome est l’une des oeuvres scientifiques de :
1. Rappel des modèles
- Thomson → modèle du « plum pudding » (pudding aux raisins)
- Rutherford → modèle nucléaire (noyau central, atome compact)
- Bohr → modèle planétaire quantifié
- Dalton → théorie atomique (billes dures)
- Planck → quantification de l’énergie (pas un modèle atomique)
2. Modèle compact
→ L’atome est essentiellement vide, mais toute la masse est concentrée dans un noyau très petit et très dense.
→ Ce modèle est dû à Rutherford (expérience de la feuille d’or).
20. Le point du programme du cours de chimie 6ème qui étudie les recouvrements des orbitales atomiques est :
Le recouvrement des orbitales atomiques est directement lié à la formation des liaisons covalentes.
→ C’est le cœur de la théorie de la liaison de valence (VB)
→ On y étudie : recouvrement s–s, s–p, p–p, hybridation, etc.
Ce contenu appartient clairement au chapitre des liaisons chimiques.
21.La théorie quantique de l’atome est l’une des oeuvres scientifiques de :
1. Rôle de Planck
Max Planck est le fondateur de la théorie des quanta (1900).
→ Il introduit l’idée que l’énergie est émise par paquets discrets : les quanta.
2. Application à l’atome
Cette idée est la base de toute la théorie quantique de l’atome,
sur laquelle Bohr construira ensuite son modèle quantifié.
Donc l’origine de la théorie quantique revient à Planck.
22.La formule chimique du produit chimique utilisé comme l’un des ingrédients dans la fabrication du savon est :
1. Réaction de saponification
→ Le savon est obtenu par réaction entre un corps gras (huile) et une base forte
→ Les bases typiques sont :
- NaOH (hydroxyde de sodium)
- Na_2CO_3 (carbonate de sodium) → utilisé comme agent alcalin dans certaines fabrications
2. Parmi les propositions
- Na_2CO_3 est bien utilisé comme ingrédient alcalin dans la fabrication du savon
- Les autres (CaO, Cl_2, NaClO, FeCl_3) ne sont pas directement impliqués dans la saponification
23.La formule chimique du produit chimique le plus communément utilisé comme désinfectant de l’eau des piscines communautaires est :
1. Produits désinfectants utilisés en piscine
→ Le chlore est le désinfectant principal, mais il est souvent utilisé sous forme de hypochlorite de sodium: \( \text{NaClO} \)
→ Il libère du chlore actif en solution, détruisant bactéries, virus et algues
2. Comparaison
- Cl_2 → trop instable et dangereux à manipuler directement
- NaClO → forme commerciale la plus courante (eau de Javel diluée)
24.Quel est le moment dipolaire électrique de la molécule HCl si la longueur de la liaison est \(1{,}26 \cdot 10^{-8}\ \text{cm}\) ?
1. Formule du moment dipolaire
\[
\mu = q \cdot d
\quad \text{avec } \mu \text{ en Debye (D)},\ d \text{ en cm},\ q \text{ en statCoulomb}
\]
2. Valeurs typiques
- Charge \(q = 4{,}8 \cdot 10^{-10}\ \text{statC}\)
- Distance \(d = 1{,}26 \cdot 10^{-8}\ \text{cm}\)
\[
\mu = 4{,}8 \cdot 10^{-10} \cdot 1{,}26 \cdot 10^{-8} = 6{,}048 \cdot 10^{-18}\ \text{esu.cm}
\]
3. Conversion en Debye
\[
1\ \text{D} = 10^{-18}\ \text{esu.cm}
\quad \Rightarrow \quad \mu = 6{,}048\ \text{D}
\]
→ La valeur la plus proche parmi les choix est :
\[
\boxed{d. 6{,}77\ \text{D}}
\]
