Exetat Chimie 2025_Scientifique
Question 1
1. Un échantillon de NaI est injecté à un patient dans le cadre du traitement d’un cancer de la thyroïde. Si l’échantillon a une radioactivité de 10,000 dés/min à 8h50’, sachant que sa période radioactive ou demi-vie est de 25 minutes. Sa radioactivité (en dés/min) à 10h05’ sera :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 1,250 dés/min (proposition c).
Explication :
La période radioactive (demi-vie) est de 25 minutes.
On passe de 8h50’ à 10h05’, soit 1h15’ = 75 minutes.
Le nombre de périodes écoulées est :
\[
n = \frac{75}{25} = 3
\]
La loi de décroissance radioactive est :
\[
A = A_0 \left(\frac{1}{2}\right)^n
\]
où \( A_0 = 10,000 \) dés/min et \( n = 3 \).
Donc :
\[
A = 10,000 \left(\frac{1}{2}\right)^3
= 10,000 \times \frac{1}{8}
= 1,250 \ \text{dés/min}
\]
La radioactivité à 10h05’ est donc :
\[
\boxed{1,250 \ \text{dés/min}}
\]
2. Pendant le tour de salles dans un centre de santé, le médecin prescrit pour un octogénaire \(2 \times 10^{21}\) molécules de l’acide acétylsalicylique ou aspirine \(\text{C}_9\text{H}_8\text{O}_4\). La masse de ce médicament (en mg) est :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 600 mg (proposition b).
Explication :
On calcule d’abord la masse molaire de l’aspirine \(\text{C}_9\text{H}_8\text{O}_4\) :
\[
M = 9 \times 12 + 8 \times 1 + 4 \times 16 = 108 + 8 + 64 = 180 \ \text{g/mol}
\]
On utilise le nombre d’Avogadro :
\[
N_A = 6{,}02 \times 10^{23} \ \text{molécules/mol}
\]
La quantité de matière correspondant à \(2 \times 10^{21}\) molécules est :
\[
n = \frac{2 \times 10^{21}}{6{,}02 \times 10^{23}} \approx 3{,}32 \times 10^{-3} \ \text{mol}
\]
La masse correspondante est :
\[
m = n \times M \approx 3{,}32 \times 10^{-3} \times 180 \approx 0{,}598 \ \text{g}
\]
En milligrammes :
\[
0{,}598 \ \text{g} \approx 598 \ \text{mg} \approx 600 \ \text{mg}
\]
Donc la masse du médicament est :
\[
\boxed{600 \ \text{mg}}
\]
3. Dans un laboratoire d’une usine de fabrication des médicaments, il est demandé de diluer deux fois une solution molaire obtenue par dissolution de 52,8 g d’acide ascorbique (ou vitamine C), de formule ci‑contre. Le volume (en litre) de la solution diluée vaut : 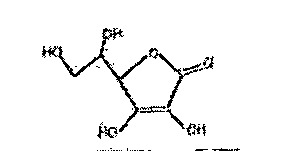
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32
Réponse correcte : 0,6 L (proposition c).
Explication :
La formule brute de l’acide ascorbique (vitamine C) est \(\text{C}_6\text{H}_8\text{O}_6\).
Sa masse molaire est :
\[
M = 6 \times 12 + 8 \times 1 + 6 \times 16 = 72 + 8 + 96 = 176 \ \text{g/mol}
\]
La quantité de matière dans 52,8 g est :
\[
n = \frac{52,8}{176} = 0,3 \ \text{mol}
\]
La solution est dite « molaire », donc sa concentration est :
\[
C = 1 \ \text{mol/L}
\]
Le volume de la solution initiale est alors :
\[
V\_{\text{initial}} = \frac{n}{C} = \frac{0,3}{1} = 0,3 \ \text{L}
\]
Diluer deux fois signifie doubler le volume (dilution au facteur 2) :
\[
V\_{\text{final}} = 2 \times V\_{\text{initial}} = 2 \times 0,3 = 0,6 \ \text{L}
\]
Donc le volume de la solution diluée est :
\[
\boxed{0,6 \ \text{L}}
\]
4. Voici ci‑contre le schéma de l’électrolyse de l’eau pour produire principalement de l’hydrogène gazeux.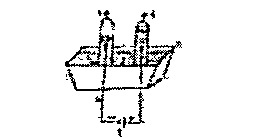
Le chiffre 3 désigne :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32
Réponse correcte : L’oxygène à recueillir (proposition b).
Explication :
Dans l’électrolyse de l’eau :
- Au niveau de la cathode (borne négative), on forme du dihydrogène \(H_2\).
- Au niveau de l’anode (borne positive), on forme du dioxygène \(O_2\).
Sur le schéma, le chiffre 3 pointe vers le tube du côté de l’anode, où se dégage le dioxygène.
Ainsi, le chiffre 3 désigne :
\[
\boxed{\text{l’oxygène à recueillir}}
\]
5. En vue d’une analyse au laboratoire, un chimiste pèse 2,2 g de soude caustique. Il ajoute de l’eau distillée et une goutte d’un indicateur coloré. La neutralisation s’obtient par adjonction de 60 ml d’une solution de l’acide sulfurique 0,3 M. Le pourcentage NaOH contenu dans cette solution est :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 65,4 % (proposition d).
Explication :
L’équation de neutralisation est :
\[
2 \text{NaOH} + \text{H}_2\text{SO}_4 \rightarrow \text{Na}_2\text{SO}_4 + 2 \text{H}_2\text{O}
\]
On calcule la quantité de matière d’acide sulfurique :
\[
n(\text{H}_2\text{SO}_4) = C \times V = 0,3 \times 0,060 = 0,018 \ \text{mol}
\]
D’après la stœchiométrie, il faut 2 moles de NaOH pour 1 mole de H2SO4 :
\[
n(\text{NaOH}) = 2 \times 0,018 = 0,036 \ \text{mol}
\]
Masse molaire de NaOH :
\[
M(\text{NaOH}) = 40 \ \text{g/mol}
\]
Masse de NaOH pur dans l’échantillon :
\[
m(\text{NaOH}) = 0,036 \times 40 = 1,44 \ \text{g}
\]
Pourcentage massique de NaOH dans les 2,2 g de soude caustique :
\[
\% \text{NaOH} = \frac{1,44}{2,2} \times 100 \approx 65,4 \ \%
\]
Donc le pourcentage de NaOH est :
\[
\boxed{65,4 \ \%}
\]
6. 6. Lors de la réaction d’oxydo‑réduction, l’acide sulfurique concentré et chaud est un agent oxydant vis‑à‑vis du mercure. On obtient des ions mercuriques et un dégagement de dioxyde de soufre. La masse de mercure à utiliser pour obtenir 3 litres de dioxyde de soufre gazeux dans les conditions normales vaut :
Réaction chimique : \(\text{Hg} + \text{H}_2\text{SO}_4 \rightarrow \text{HgSO}_4 + \text{SO}_2 + \text{H}_2\text{O}\).
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 26,86 g (proposition b).
Explication :
Dans l’équation donnée, il y a proportion stœchiométrique :
\[
\text{Hg} \longrightarrow \text{SO}_2
\]
Donc 1 mole de Hg produit 1 mole de SO2.
À conditions normales, le volume molaire d’un gaz est :
\[
V_m = 22,4 \ \text{L/mol}
\]
La quantité de matière de SO2 correspondant à 3 L est :
\[
n(\text{SO}_2) = \frac{3}{22,4} \approx 0,134 \ \text{mol}
\]
Par stœchiométrie :
\[
n(\text{Hg}) = n(\text{SO}_2) \approx 0,134 \ \text{mol}
\]
La masse molaire du mercure est :
\[
M(\text{Hg}) = 200,59 \ \text{g/mol}
\]
La masse de Hg nécessaire est donc :
\[
m(\text{Hg}) = n \times M \approx 0,134 \times 200,59 \approx 26,86 \ \text{g}
\]
Donc la masse de mercure requise est :
\[
\boxed{26,86 \ \text{g}}
\]
7. Un échantillon de NaI est injecté à un patient dans le cadre du traitement d’un cancer de la thyroïde. Si l’échantillon a une radioactivité de 10000 dés/min à 10h05’, sachant que sa période radioactive ou demi-vie est de 25 minutes. Sa radioactivité (en dés/min) à 11h45’ sera :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 625 dés/min (proposition b).
Explication :
De 10h05’ à 11h45’, il s’écoule 1h40’, soit 100 minutes.
Le nombre de périodes radioactives est :
\[
n = \frac{100}{25} = 4
\]
La loi de décroissance radioactive est :
\[
A = A_0 \left(\frac{1}{2}\right)^n
\]
avec \(A_0 = 10000\) dés/min et \(n = 4\).
Donc :
\[
A = 10000 \left(\frac{1}{2}\right)^4
= 10000 \times \frac{1}{16}
= 625 \ \text{dés/min}
\]
La radioactivité à 11h45’ est donc :
\[
\boxed{625 \ \text{dés/min}}
\]
8. Dans un laboratoire d’une usine de fabrication des médicaments, il est demandé de diluer deux fois une solution molaire obtenue par dissolution de 70,4 g d’acide ascorbique (ou vitamine C), de formule ci‑contre.
Le volume (en litre) de la solution diluée vaut :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 0,8 L (proposition d).
Explication :
La formule brute de l’acide ascorbique est \(\text{C}_6\text{H}_8\text{O}_6\).
Sa masse molaire est :
\[
M = 6 \times 12 + 8 \times 1 + 6 \times 16 = 72 + 8 + 96 = 176 \ \text{g/mol}
\]
La quantité de matière dans 70,4 g est :
\[
n = \frac{70,4}{176} = 0,4 \ \text{mol}
\]
La solution est « molaire », donc :
\[
C = 1 \ \text{mol/L}
\]
Le volume de la solution initiale est :
\[
V_{\text{initial}} = \frac{n}{C} = \frac{0,4}{1} = 0,4 \ \text{L}
\]
Diluer deux fois signifie doubler le volume :
\[
V_{\text{final}} = 2 \times 0,4 = 0,8 \ \text{L}
\]
Donc le volume de la solution diluée est :
\[
\boxed{0,8 \ \text{L}}
\]
9. Voici ci‑contre le schéma de l’électrolyse de l’eau pour produire principalement de l’hydrogène gazeux.
Le chiffre 2 désigne :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : L’hydrogène à recueillir (proposition a).
Explication :
Lors de l’électrolyse de l’eau :
- À la cathode (borne négative), il y a réduction de l’eau avec dégagement de dihydrogène \(H_2\).
- À l’anode (borne positive), il y a oxydation de l’eau avec dégagement de dioxygène \(O_2\).
Sur le schéma, le chiffre 2 pointe vers le tube où se forme le gaz produit en plus grande quantité, c’est‑à‑dire le dihydrogène.
Ainsi, le chiffre 2 désigne :
\[
\boxed{\text{l’hydrogène à recueillir}}
\]
10. En vue d’une analyse au laboratoire, un chimiste pèse 2,5 g de soude caustique. Il ajoute de l’eau distillée et une goutte d’un indicateur coloré. La neutralisation s’obtient par adjonction de 60 ml d’une solution de l’acide sulfurique 0,3 M. Le pourcentage NaOH contenu dans cette solution est :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 58,0 % (proposition a).
Explication :
L’équation de neutralisation est :
\[
2 \text{NaOH} + \text{H}_2\text{SO}_4 \rightarrow \text{Na}_2\text{SO}_4 + 2 \text{H}_2\text{O}
\]
Quantité de matière d’acide sulfurique :
\[
n(\text{H}_2\text{SO}_4) = C \times V = 0,3 \times 0,060 = 0,018 \ \text{mol}
\]
D’après la stœchiométrie, il faut 2 moles de NaOH pour 1 mole de H2SO4 :
\[
n(\text{NaOH}) = 2 \times 0,018 = 0,036 \ \text{mol}
\]
Masse molaire de NaOH :
\[
M(\text{NaOH}) = 40 \ \text{g/mol}
\]
Masse de NaOH pur dans l’échantillon :
\[
m(\text{NaOH}) = 0,036 \times 40 = 1,44 \ \text{g}
\]
Pourcentage massique de NaOH dans les 2,5 g de soude caustique :
\[
\% \text{NaOH} = \frac{1,44}{2,5} \times 100 \approx 57,6 \ \% \approx 58,0 \ \%
\]
Donc le pourcentage de NaOH est :
\[
\boxed{58,0 \ \%}
\]
Lors de la réaction d’oxydo‑réduction, l’acide sulfurique concentré et chaud est un agent oxydant vis‑à‑vis du mercure. On obtient des ions mercuriques et un dégagement de dioxyde de soufre. La masse de mercure à utiliser pour obtenir 4 litres de dioxyde de soufre gazeux dans les conditions normales vaut :Réaction chimique : \(\text{Hg} + \text{H}_2\text{SO}_4 \rightarrow \text{HgSO}_4 + \text{SO}_2 + \text{H}_2\text{O}\).
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 35,82 g (proposition c).
Explication :
D’après l’équation :
\[
\text{Hg} \rightarrow \text{SO}_2
\]
1 mole de Hg donne 1 mole de SO2.
À conditions normales, le volume molaire d’un gaz est :
\[
V_m = 22,4 \ \text{L/mol}
\]
La quantité de matière de SO2 pour 4 L est :
\[
n(\text{SO}_2) = \frac{4}{22,4} \approx 0,179 \ \text{mol}
\]
Donc :
\[
n(\text{Hg}) = n(\text{SO}_2) \approx 0,179 \ \text{mol}
\]
Masse molaire du mercure :
\[
M(\text{Hg}) = 200,59 \ \text{g/mol}
\]
Masse de Hg nécessaire :
\[
m(\text{Hg}) = n \times M \approx 0,179 \times 200,59 \approx 35,82 \ \text{g}
\]
Donc la masse de mercure à utiliser est :
\[
\boxed{35,82 \ \text{g}}
\]
12. Pendant le tour de salles dans un centre de santé, le médecin prescrit pour un adolescent \(1{,}5 \times 10^{21}\) molécules de l’acide acétylsalicylique ou aspirine \(\text{C}_9\text{H}_8\text{O}_4\). La masse de ce médicament (en mg) est :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Réponse correcte : 500 mg (proposition c).
Explication :
On calcule la masse molaire de l’aspirine \(\text{C}_9\text{H}_8\text{O}_4\) :
\[
M = 9 \times 12 + 8 \times 1 + 4 \times 16 = 108 + 8 + 64 = 180 \ \text{g/mol}
\]
On utilise le nombre d’Avogadro :
\[
N_A = 6{,}02 \times 10^{23} \ \text{molécules/mol}
\]
La quantité de matière correspondant à \(1{,}5 \times 10^{21}\) molécules est :
\[
n = \frac{1{,}5 \times 10^{21}}{6{,}02 \times 10^{23}} \approx 2{,}49 \times 10^{-3} \ \text{mol}
\]
La masse correspondante est :
\[
m = n \times M \approx 2{,}49 \times 10^{-3} \times 180 \approx 0{,}448 \ \text{g}
\]
En milligrammes :
\[
0{,}448 \ \text{g} \approx 448 \ \text{mg} \approx 500 \ \text{mg}
\]
Donc la masse du médicament est :
\[
\boxed{500 \ \text{mg}}
\]
13. Lors de la fabrication des engrais chimiques dans une industrie, un chimiste prépare 9 l d’acide sulfurique 0,1 N. Le volume de l’acide sulfurique concentré (95 % et masse volumique 1,8 g/ml) qu’il faut diluer est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Réponse correcte : 25,7 ml (proposition c).
Explication :
L’acide sulfurique H₂SO₄ est dibasique, donc :
\[
N = 2C \Rightarrow C = \frac{N}{2} = \frac{0,1}{2} = 0,05 \ \text{mol/l}
\]
Quantité de matière d’H₂SO₄ dans 9 l de solution 0,1 N :
\[
n = C \times V = 0,05 \times 9 = 0,45 \ \text{mol}
\]
Masse molaire de H₂SO₄ :
\[
M = 2 \times 1 + 32 + 4 \times 16 = 98 \ \text{g/mol}
\]
Masse d’H₂SO₄ pur nécessaire :
\[
m_{\text{pur}} = n \times M = 0,45 \times 98 = 44,1 \ \text{g}
\]
La solution concentrée est à 95 % :
\[
m_{\text{solution}} = \frac{m_{\text{pur}}}{0,95} \approx \frac{44,1}{0,95} \approx 46,4 \ \text{g}
\]
Avec une masse volumique de 1,8 g/ml :
\[
V = \frac{m_{\text{solution}}}{\rho} \approx \frac{46,4}{1,8} \approx 25,8 \ \text{ml} \approx 25,7 \ \text{ml}
\]
Donc le volume d’acide sulfurique concentré à diluer est :
\[
\boxed{25,7 \ \text{ml}}
\]
14.Un chasseur a retrouvé dans une forêt le crâne d’un homme dont la quantité de carbone‑14 est 4 fois moins que celle rencontrée dans une personne vivante.
L’âge approximatif de l’être humain ayant vécu dans cette forêt est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Réponse correcte : 11440 ans (proposition d).
Explication :
La quantité de carbone‑14 est 4 fois plus faible que chez un vivant, donc :
\[
\frac{N}{N_0} = \frac{1}{4} = \left(\frac{1}{2}\right)^2
\]
Cela signifie qu’il s’est écoulé 2 périodes radioactives.
La période du carbone‑14 est de 5700 ans, donc :
\[
t = 2 \times 5700 = 11400 \ \text{ans} \approx 11440 \ \text{ans}
\]
L’âge approximatif de l’être humain est donc :
\[
\boxed{11440 \ \text{ans}}
\]
15. Un volume de 1,0 l d’une solution d’eau oxygénée produit, lors de sa décomposition spontanée, 110 l de dioxygène sous une pression de 1,0 bar et à une température de 0 °C.
Réaction : \(\text{H}_2\text{O}_2 \rightarrow \text{H}_2\text{O} + \tfrac{1}{2}\text{O}_2\)
La quantité de dioxygène produite lors de la décomposition de \(V_0 = 0,16\) l de cette solution d’eau oxygénée est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Réponse correcte : 1,5 mol (proposition c).
Explication :
De 1,0 l de solution, on obtient 110 l de \(\text{O}_2\).
De 0,16 l de solution, le volume de \(\text{O}_2\) est donc :
\[
V(\text{O}_2) = 110 \times 0,16 = 17,6 \ \text{l}
\]
À 0 °C et 1 bar, on peut prendre \(V_m \approx 22,4 \ \text{l/mol}\), donc :
\[
n(\text{O}_2) = \frac{17,6}{22,4} \approx 0,79 \ \text{mol}
\]
D’après la réaction \(\text{H}_2\text{O}_2 \rightarrow \text{H}_2\text{O} + \tfrac{1}{2}\text{O}_2\),
2 moles de \(\text{H}_2\text{O}_2\) donnent 1 mole de \(\text{O}_2\), donc :
\[
n(\text{H}_2\text{O}_2) = 2 \times n(\text{O}_2) \approx 2 \times 0,79 \approx 1,58 \ \text{mol} \approx 1,5 \ \text{mol}
\]
On obtient ainsi :
\[
\boxed{1,5 \ \text{mol}}
\]
16. Selon la loi de Faraday en électrolyse : « La quantité des substances obtenues aux électrodes est proportionnelle à la quantité de courant utilisé ».
La masse de zinc déposée en 2 heures à la cathode d’un voltamètre à sulfate de zinc lorsqu’il est traversé par un courant de 0,5 A est égale à :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Réponse correcte : 1,21 g (proposition c).
Explication :
La demi‑équation à la cathode est :
\[
\text{Zn}^{2+} + 2 e^- \rightarrow \text{Zn}
\]
La charge électrique passée est :
\[
Q = I \times t = 0,5 \times (2 \times 3600) = 3600 \ \text{C}
\]
La quantité d’électricité correspondant à 1 mole d’électrons est la constante de Faraday :
\[
F = 9,65 \times 10^{4} \ \text{C/mol}
\]
Quantité de matière d’électrons :
\[
n(e^-) = \frac{Q}{F} = \frac{3600}{9,65 \times 10^{4}} \approx 3,73 \times 10^{-2} \ \text{mol}
\]
Il faut 2 moles d’électrons pour déposer 1 mole de Zn :
\[
n(\text{Zn}) = \frac{n(e^-)}{2} \approx \frac{3,73 \times 10^{-2}}{2} \approx 1,87 \times 10^{-2} \ \text{mol}
\]
Avec \(M(\text{Zn}) = 65,4 \ \text{g/mol}\) :
\[
m(\text{Zn}) = n \times M \approx 1,87 \times 10^{-2} \times 65,4 \approx 1,22 \ \text{g} \approx 1,21 \ \text{g}
\]
Donc la masse de zinc déposée est :
\[
\boxed{1,21 \ \text{g}}
\]
17. Lors d’un dosage de 10 ml de \(\text{H}_2\text{SO}_4\) 0,1 N par une solution de \(\text{Ca(OH)}_2\) 0,1 N, après avoir laissé couler goutte à goutte un volume précis de la base, la masse du sel formé est de 0,034 g.
Le volume de la solution basique correspondant à cette masse est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Réponse correcte : 5 ml (proposition b).
Explication :
L’équation de réaction est :
\[
\text{H}_2\text{SO}_4 + \text{Ca(OH)}_2 \rightarrow \text{CaSO}_4 + 2 \text{H}_2\text{O}
\]
Le sel formé est le sulfate de calcium \(\text{CaSO}_4\).
Sa masse molaire est :
\[
M(\text{CaSO}_4) = 40 + 32 + 4 \times 16 = 136 \ \text{g/mol}
\]
La quantité de matière de sel formé est :
\[
n(\text{CaSO}_4) = \frac{0,034}{136} = 2,5 \times 10^{-4} \ \text{mol}
\]
D’après l’équation, 1 mole de \(\text{Ca(OH)}_2\) donne 1 mole de \(\text{CaSO}_4\), donc :
\[
n(\text{Ca(OH)}_2) = 2,5 \times 10^{-4} \ \text{mol}
\]
La normalité de \(\text{Ca(OH)}_2\) est 0,1 N. Comme \(\text{Ca(OH)}_2\) fournit 2 OH⁻, sa molarité vaut :
\[
C = \frac{N}{2} = \frac{0,1}{2} = 0,05 \ \text{mol/l}
\]
Le volume de base utilisé est alors :
\[
V = \frac{n}{C} = \frac{2,5 \times 10^{-4}}{0,05} = 5 \times 10^{-3} \ \text{l} = 5 \ \text{ml}
\]
Donc le volume de la solution basique correspondant à cette masse est :
\[
\boxed{5 \ \text{ml}}
\]
18. Un chimiste reçoit quatre bouteilles d’un litre de solution d’acide de batterie (\(\text{H}_2\text{SO}_4\)). Voulant connaître la masse de l’acide pur contenu dans chaque bouteille, il prélève 50 ml de chaque bouteille et les titre par une solution de \(\text{NaOH}\). Il sort du laboratoire avec les graphiques ci‑dessous.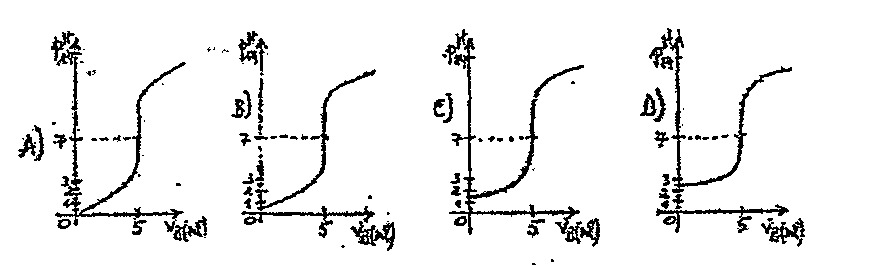
Après analyse et interprétation de ces graphiques, la masse en gramme de l’acide contenu dans la solution utilisée au graphique B vaut :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Réponse correcte : 0,2450 g (proposition c).
Explication :
Au point d’équivalence, on a l’égalité des équivalents :
\[
N_{\text{acide}} V_{\text{acide}} = N_{\text{base}} V_{\text{base}}
\]
L’acide sulfurique est dibasique, donc :
\[
N_{\text{acide}} = 2 C_{\text{acide}}
\]
On sait que la masse d’acide pur peut se mettre sous la forme (en utilisant la normalité de la base et le volume à l’équivalence) :
\[
m(\text{H}_2\text{SO}_4) = \frac{N_{\text{base}} \, V_{\text{base,\,eq}} \, M(\text{H}_2\text{SO}_4)}{2}
\]
Avec :
\[
N_{\text{base}} = 0,1 \ \text{N}, \quad V_{\text{base,\,eq}} = 50 \ \text{ml} = 0,050 \ \text{l}, \quad M(\text{H}_2\text{SO}_4) = 98 \ \text{g/mol}
\]
On obtient :
\[
m = \frac{0,1 \times 0,050 \times 98}{2} = 0,245 \ \text{g}
\]
Donc la masse d’acide dans la solution correspondant au graphique B est :
\[
\boxed{0,2450 \ \text{g}}
\]
19. Lors de la fabrication des engrais chimiques dans une industrie, un chimiste prépare 8 l d’acide sulfurique 0,1 N.
Le volume de l’acide sulfurique concentré (95 % et masse volumique 1,8 g/ml) qu’il faut diluer est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Lors de la fabrication des engrais chimiques dans une industrie, un chimiste prépare 8 l d’acide sulfurique 0,1 N. Le volume de l’acide sulfurique concentré (95 % et masse volumique 1,8 g/ml) qu’il faut diluer est :
20. Un chasseur a retrouvé dans une forêt le crâne d’un homme dont la quantité de carbone‑14 est 6 fois moins que celle rencontrée dans une personne vivante.
L’âge approximatif de l’être humain ayant vécu dans cette forêt est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Réponse correcte : 14872 ans (proposition b).
Explication :
La quantité de carbone‑14 est 6 fois plus faible que chez un vivant, donc :
\[
\frac{N}{N_0} = \frac{1}{6}
\]
La loi de décroissance radioactive s’écrit :
\[
\frac{N}{N_0} = \left(\frac{1}{2}\right)^{t/T}
\]
où \(T = 5700\) ans est la période du carbone‑14.
On a donc :
\[
\left(\frac{1}{2}\right)^{t/T} = \frac{1}{6}
\quad \Rightarrow \quad
\frac{t}{T} = \frac{\ln(1/6)}{\ln(1/2)} \approx 2{,}61
\]
Ainsi :
\[
t \approx 2{,}61 \times 5700 \approx 14870 \ \text{ans} \approx 14872 \ \text{ans}
\]
L’âge approximatif de l’être humain est donc :
\[
\boxed{14872 \ \text{ans}}
\]
21.Un volume de 1,0 l d’une solution d’eau oxygénée produit, lors de sa décomposition spontanée, 110 l de dioxygène sous une pression de 1,0 bar et à une température de 0 °C.
Réaction : \(\text{H}_2\text{O}_2 \rightarrow \text{H}_2\text{O} + \tfrac{1}{2}\text{O}_2\).
La quantité de dioxygène produite lors de la décomposition de \(V_0 = 0,17\) l de cette solution d’eau oxygénée est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Réponse correcte : 1,7 mol (proposition e).
Explication :
De 1,0 l de solution, on obtient 110 l de \(\text{O}_2\).
De 0,17 l de solution, le volume de \(\text{O}_2\) est donc :
\[
V(\text{O}_2) = 110 \times 0,17 = 18,7 \ \text{l}
\]
À 0 °C et 1 bar, on prend \(V_m \approx 22,4 \ \text{l/mol}\), donc :
\[
n(\text{O}_2) = \frac{18,7}{22,4} \approx 0,835 \ \text{mol}
\]
D’après la réaction \(\text{H}_2\text{O}_2 \rightarrow \text{H}_2\text{O} + \tfrac{1}{2}\text{O}_2\),
2 moles de \(\text{H}_2\text{O}_2\) donnent 1 mole de \(\text{O}_2\), donc :
\[
n(\text{H}_2\text{O}_2) = 2 \times n(\text{O}_2) \approx 2 \times 0,835 \approx 1,67 \ \text{mol} \approx 1,7 \ \text{mol}
\]
On obtient ainsi :
\[
\boxed{1,7 \ \text{mol}}
\]
22. Selon la loi de Faraday en électrolyse : « La quantité des substances obtenues aux électrodes est proportionnelle à la quantité de courant utilisé ».
La masse de zinc déposée en 2 heures à la cathode d’un voltamètre à sulfate de zinc lorsqu’il est traversé par un courant de 0,6 A est égale à :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Réponse correcte : 1,45 g (proposition d).
Explication :
La demi‑équation à la cathode est :
\[
\text{Zn}^{2+} + 2 e^- \rightarrow \text{Zn}
\]
La charge électrique passée est :
\[
Q = I \times t = 0,6 \times (2 \times 3600) = 4320 \ \text{C}
\]
La quantité d’électricité correspondant à 1 mole d’électrons est la constante de Faraday :
\[
F = 9,65 \times 10^{4} \ \text{C/mol}
\]
Quantité de matière d’électrons :
\[
n(e^-) = \frac{Q}{F} = \frac{4320}{9,65 \times 10^{4}} \approx 4,48 \times 10^{-2} \ \text{mol}
\]
Il faut 2 moles d’électrons pour déposer 1 mole de Zn :
\[
n(\text{Zn}) = \frac{n(e^-)}{2} \approx \frac{4,48 \times 10^{-2}}{2} \approx 2,24 \times 10^{-2} \ \text{mol}
\]
Avec \(M(\text{Zn}) = 65,4 \ \text{g/mol}\) :
\[
m(\text{Zn}) = n \times M \approx 2,24 \times 10^{-2} \times 65,4 \approx 1,47 \ \text{g} \approx 1,45 \ \text{g}
\]
Donc la masse de zinc déposée est :
\[
\boxed{1,45 \ \text{g}}
\]
23. Lors d’un dosage de 10 ml de \(\text{H}_2\text{SO}_4\) 0,1 N par une solution de \(\text{Ca(OH)}_2\) 0,1 N, après avoir laissé couler goutte à goutte un volume précis de la base, la masse du sel formé est de 0,054 g.
Le volume de la solution basique correspondant à cette masse est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Réponse correcte : 8 ml (proposition d).
Explication :
La réaction de neutralisation est :
\[
\text{H}_2\text{SO}_4 + \text{Ca(OH)}_2 \rightarrow \text{CaSO}_4 + 2\text{H}_2\text{O}
\]
Le sel formé est le sulfate de calcium \(\text{CaSO}_4\).
Sa masse molaire vaut :
\[
M(\text{CaSO}_4) = 40 + 32 + 4 \times 16 = 136 \ \text{g/mol}
\]
Quantité de matière de sel formé :
\[
n(\text{CaSO}_4) = \frac{0,054}{136} = 3,97 \times 10^{-4} \ \text{mol}
\]
D’après l’équation, 1 mole de \(\text{Ca(OH)}_2\) donne 1 mole de \(\text{CaSO}_4\), donc :
\[
n(\text{Ca(OH)}_2) = 3,97 \times 10^{-4} \ \text{mol}
\]
La normalité de \(\text{Ca(OH)}_2\) est 0,1 N. Comme la base fournit 2 OH⁻ :
\[
C = \frac{N}{2} = \frac{0,1}{2} = 0,05 \ \text{mol/l}
\]
Volume de base utilisé :
\[
V = \frac{n}{C} = \frac{3,97 \times 10^{-4}}{0,05}
= 7,94 \times 10^{-3} \ \text{l}
= 7,94 \ \text{ml} \approx 8 \ \text{ml}
\]
Donc le volume correspondant est :
\[
\boxed{8 \ \text{ml}}
\]
24. Un chimiste reçoit quatre bouteilles d’un litre de solution d’acide de batterie (\(\text{H}_2\text{SO}_4\)). Voulant connaître la masse de l’acide pur contenu dans chaque bouteille, il prélève 50 ml de chaque bouteille et les titre par une solution de \(\text{NaOH}\). Il sort du laboratoire avec les graphiques ci‑dessous.
Après analyse et interprétation de ces graphiques, la masse en gramme de l’acide contenue dans la solution utilisée au graphique A vaut :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Réponse correcte : 0,0735 g (proposition b).
Explication :
Au point d’équivalence, on a l’égalité des équivalents :
\[
N_{\text{acide}} V_{\text{acide}} = N_{\text{base}} V_{\text{base,\,eq}}
\]
L’acide sulfurique est dibasique, donc :
\[
N_{\text{acide}} = 2 C_{\text{acide}}
\]
La masse d’acide pur peut se calculer à partir de la normalité de la base, du volume à l’équivalence
et de la masse molaire de \(\text{H}_2\text{SO}_4\) :
\[
m(\text{H}_2\text{SO}_4) = \frac{N_{\text{base}} \, V_{\text{base,\,eq}} \, M(\text{H}_2\text{SO}_4)}{2}
\]
Pour le graphique A, on lit à l’équivalence :
\[
V_{\text{base,\,eq}} = 15 \ \text{ml} = 0,015 \ \text{l}
\]
Avec :
\[
N_{\text{base}} = 0,1 \ \text{N}, \quad M(\text{H}_2\text{SO}_4) = 98 \ \text{g/mol}
\]
On obtient :
\[
m = \frac{0,1 \times 0,015 \times 98}{2} = 0,0735 \ \text{g}
\]
Donc la masse d’acide contenue dans la solution correspondant au graphique A est :
\[
\boxed{0,0735 \ \text{g}}
\]
25.100 ml d’un vin contenant 9,0 ml d’éthanol de masse volumique \(\rho = 790 \ \text{kg·m}^{-3}\), abandonné à l’air, s’oxyde et se transforme en vinaigre selon l’équation chimique ci‑après : \[ \text{CH}_3\text{CH}_2\text{OH} + \text{O}_2 \rightarrow \text{CH}_3\text{COOH} + \text{H}_2\text{O} \] La masse maximale d’acide formée lors de la transformation d’un litre de vin à 10^\circ\text{C} vaut :
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Réponse correcte : 92,7 g (proposition b).
Explication :
Dans 100 ml de vin, il y a 9,0 ml d’éthanol.
Dans 1,0 l de vin (soit 10 fois plus), le volume d’éthanol est donc :
\[
V_{\text{EtOH}} = 10 \times 9,0 = 90 \ \text{ml}
\]
Avec \(\rho = 790 \ \text{kg·m}^{-3} = 0,79 \ \text{g·ml}^{-1}\), la masse d’éthanol vaut :
\[
m_{\text{EtOH}} = 0,79 \times 90 = 71,1 \ \text{g}
\]
Masse molaire de l’éthanol \(\text{CH}_3\text{CH}_2\text{OH}\) :
\[
M_{\text{EtOH}} = 2 \times 12 + 6 \times 1 + 16 = 46 \ \text{g·mol}^{-1}
\]
Quantité de matière d’éthanol :
\[
n_{\text{EtOH}} = \frac{71,1}{46} \approx 1,55 \ \text{mol}
\]
L’équation montre un rapport 1:1 entre l’éthanol et l’acide acétique \(\text{CH}_3\text{COOH}\).
Masse molaire de l’acide acétique :
\[
M_{\text{acide}} = 2 \times 12 + 4 \times 1 + 2 \times 16 = 60 \ \text{g·mol}^{-1}
\]
Masse maximale d’acide formée :
\[
m_{\text{acide}} = n_{\text{EtOH}} \times M_{\text{acide}} \approx 1,55 \times 60 \approx 93 \ \text{g} \approx 92,7 \ \text{g}
\]
Donc :
\[
\boxed{m_{\text{acide}} \approx 92,7 \ \text{g}}
\]
26. En médecine, les atomes radioactifs sont utilisés comme source de rayonnement.
Parmi les éléments ci‑dessous, lesquels déterminent le volume du sang que contient le corps humain.
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Réponse correcte : Na–24 (proposition c).
Explication :
En médecine nucléaire, le \(\text{Na–24}\) (sodium‑24) est utilisé comme traceur pour étudier la circulation sanguine
et déterminer le volume sanguin total, car le sodium se répartit rapidement et de manière homogène dans le
compartiment sanguin.
Les isotopes de l’iode (\(I_{131}, I_{132}\)) sont surtout utilisés pour la thyroïde, le Co–60 pour la radiothérapie,
le Pu–238 comme source énergétique et non comme traceur biologique, et le Zn–30 n’est pas utilisé pour mesurer
le volume sanguin.
Ainsi, l’isotope adapté à la détermination du volume de sang est :
\[
\boxed{\text{Na–24}}
\]
27. Soit le spectre de la lumière :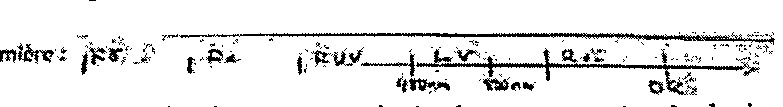
La lumière est constituée des composantes à plusieurs longueurs d’onde (\(\lambda\)) allant du rayon gamma (\(\gamma\)) jusqu’aux ondes radio (OR).
L’énergie de liaison simple C–C dans le composé \(\text{C}_6\text{H}_6 (g)\) est égale à \(345 \ \text{kJ·mol}^{-1}\).
La longueur d’onde de la lumière capable de transformer l’éthane en méthane selon cette équation chimique :
\[ \text{C}_2\text{H}_6 (g) \rightarrow 2 \text{CH}_4 \]
vaut… et est située dans :
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Réponse correcte : 344 nm et dans l’ultraviolet (proposition b).
Explication :
L’énergie de liaison C–C est :
\[
E_{\text{liaison}} = 345 \ \text{kJ·mol}^{-1} = 345000 \ \text{J·mol}^{-1}
\]
L’énergie d’un photon est :
\[
E = \frac{h c}{\lambda}
\]
et pour une mole de photons :
\[
E_{\text{mol}} = N_A \frac{h c}{\lambda}
\]
Donc :
\[
\lambda = \frac{N_A h c}{E_{\text{mol}}}
\]
Avec :
\[
h = 6{,}625 \times 10^{-34} \ \text{J·s}, \quad
c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}, \quad
N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}
\]
On obtient numériquement :
\[
\lambda \approx 3{,}4 \times 10^{-7} \ \text{m} = 340 \ \text{nm} \ (\text{ordre de grandeur})
\]
Cette longueur d’onde est dans le domaine de l’ultraviolet (environ 10–400 nm).
La valeur proposée la plus proche et correctement située dans l’UV est :
\[
\boxed{344 \ \text{nm} \ \text{et dans l’ultraviolet (UV)}}
\]
28. On dissout 0,532 g de \(\text{IO}_3\), sel oxydant, dans l’eau distillée pour obtenir 300 ml de solution. Sachant que le couple oxydo‑réducteur est \(\text{IO}_3^-/\text{I}_2\).
La normalité de la solution préparée est :
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Réponse correcte : 0,04 éq/l (proposition d).
Explication :
Le sel oxydant est pris comme \(\text{KIO}_3\).
Sa masse molaire est :
\[
M(\text{KIO}_3) = 39 + 127 + 3 \times 16 = 214 \ \text{g·mol}^{-1}
\]
Quantité de matière dissoute :
\[
n = \frac{0,532}{214} \approx 2,49 \times 10^{-3} \ \text{mol}
\]
Volume de solution :
\[
V = 300 \ \text{ml} = 0,300 \ \text{l}
\]
Molarité :
\[
C = \frac{n}{V} = \frac{2,49 \times 10^{-3}}{0,300} \approx 8,3 \times 10^{-3} \ \text{mol·l}^{-1}
\]
Pour le couple \(\text{IO}_3^-/\text{I}_2\), la demi‑équation globale donne 5 électrons échangés par mole de \(\text{IO}_3^-\),
donc le facteur de valence est 5.
La normalité vaut alors :
\[
N = C \times 5 \approx 8,3 \times 10^{-3} \times 5 \approx 4,15 \times 10^{-2} \ \text{éq·l}^{-1} \approx 0,04 \ \text{éq/l}
\]
Donc :
\[
\boxed{N \approx 0,04 \ \text{éq/l}}
\]
29. Au laboratoire de l’ITA/Mombele, Paul fait réagir 300 ml de l’acide benzoïque \(0{,}5 \ \text{mol·l}^{-1} \ (C_6H_5CO_2H), \ pK_a = 4{,}2\) avec 700 ml d’une solution d’hydroxyde de sodium décimolaire.
Le \(pH\) du mélange vaut :
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Réponse correcte : 4,1 (proposition e).
Explication :
On note l’acide benzoïque \(HA\) et sa base conjuguée \(A^-\).
\[
HA + OH^- \rightarrow A^- + H_2O
\]
Quantités initiales :
\[
n(HA) = C \times V = 0{,}5 \times 0{,}300 = 0{,}15 \ \text{mol}
\]
\[
n(OH^-) = 0{,}1 \times 0{,}700 = 0{,}07 \ \text{mol}
\]
La base est limitante, elle consomme 0,07 mol de \(HA\) :
\[
n(HA)_{\text{final}} = 0{,}15 - 0{,}07 = 0{,}08 \ \text{mol}
\]
\[
n(A^-)_{\text{final}} = 0{,}07 \ \text{mol}
\]
Volume total :
\[
V_{\text{tot}} = 0{,}300 + 0{,}700 = 1{,}0 \ \text{l}
\]
Concentrations dans le mélange :
\[
[HA] = \frac{0{,}08}{1{,}0} = 0{,}08 \ \text{mol·l}^{-1}, \quad
[A^-] = \frac{0{,}07}{1{,}0} = 0{,}07 \ \text{mol·l}^{-1}
\]
On a un tampon \(HA/A^-\), donc on utilise l’équation de Henderson–Hasselbalch :
\[
pH = pK_a + \log \left( \frac{[A^-]}{[HA]} \right)
= 4{,}2 + \log \left( \frac{0{,}07}{0{,}08} \right)
\]
\[
\frac{0{,}07}{0{,}08} = 0{,}875 \quad \Rightarrow \quad \log(0{,}875) \approx -0{,}06
\]
\[
pH \approx 4{,}2 - 0{,}06 = 4{,}14 \approx 4{,}1
\]
Donc :
\[
\boxed{pH \approx 4{,}1}
\]
30. Au laboratoire, lors de la saponification, on prépare 20 ml d’une solution de soude caustique 0,2 N. On y ajoute 40 ml d’eau.
La concentration de la nouvelle solution est :
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Réponse correcte : 0,06 éq/l (proposition c).
Explication :
On utilise la relation de dilution :
\[
N_1 V_1 = N_2 V_2
\]
Données :
\[
N_1 = 0{,}2 \ \text{éq/l}, \quad V_1 = 20 \ \text{ml}, \quad V_2 = 20 + 40 = 60 \ \text{ml}
\]
Donc :
\[
N_2 = \frac{N_1 V_1}{V_2} = \frac{0{,}2 \times 20}{60}
= \frac{4}{60} \approx 0{,}0667 \ \text{éq/l} \approx 0{,}06 \ \text{éq/l}
\]
Ainsi, la concentration de la nouvelle solution est :
\[
\boxed{0{,}06 \ \text{éq/l}}
\]
31. Le permanganate de potassium réagit avec le bromure de potassium en milieu acide sulfurique pour donner le sulfate de manganèse (II), le sulfate de potassium, le brome et l’eau.
Les coefficients stœchiométriques de cette réaction sont :
Réponse correcte : 5|2|6||2|2|5|8 (proposition d).
Explication :
La réaction s’écrit sous forme ionique en milieu acide :
Oxydation du bromure :
\[
2Br^- \rightarrow Br_2 + 2e^-
\]
Réduction du permanganate :
\[
MnO_4^- + 8H^+ + 5e^- \rightarrow Mn^{2+} + 4H_2O
\]
Pour équilibrer les électrons :
\[
\text{Oxydation} \times 5 \quad \text{et} \quad \text{Réduction} \times 2
\]
On obtient :
\[
2MnO_4^- + 16H^+ + 10Br^- \rightarrow 2Mn^{2+} + 8H_2O + 5Br_2
\]
En réintroduisant les ions potassium et sulfate :
\[
2KMnO_4 + 10KBr + 8H_2SO_4 \rightarrow
2MnSO_4 + 6K_2SO_4 + 5Br_2 + 8H_2O
\]
Les coefficients sont donc :
\[
5\|2\|6\|2\|2\|5\|8
\]
Ce qui correspond à la proposition :
\[
\boxed{d}
\]
32. Un bijoutier désire fabriquer des bracelets en cuivre. En vue de purifier le cuivre brut de ses impuretés, il amène le minerai chez un chimiste. Celui-ci réalise une électrolyse avec une solution aqueuse du sulfate de cuivre (II). La masse du cuivre déposée à la cathode en 30 minutes avec un courant de 1,5 ampère est :
Réponse correcte : 0,89 g (proposition e).
Explication :
À la cathode, la demi‑équation est :
\[
\text{Cu}^{2+} + 2e^- \rightarrow \text{Cu}
\]
La charge électrique passée est :
\[
Q = I \times t = 1{,}5 \times (30 \times 60) = 1{,}5 \times 1800 = 2700 \ \text{C}
\]
La quantité de matière d’électrons est :
\[
n(e^-) = \frac{Q}{F} = \frac{2700}{9{,}65 \times 10^{4}} \approx 2{,}8 \times 10^{-2} \ \text{mol}
\]
Il faut 2 moles d’électrons pour déposer 1 mole de cuivre :
\[
n(\text{Cu}) = \frac{n(e^-)}{2} \approx \frac{2{,}8 \times 10^{-2}}{2} \approx 1{,}4 \times 10^{-2} \ \text{mol}
\]
Avec \(M(\text{Cu}) \approx 63{,}5 \ \text{g·mol}^{-1}\) :
\[
m(\text{Cu}) = n \times M \approx 1{,}4 \times 10^{-2} \times 63{,}5 \approx 0{,}89 \ \text{g}
\]
Donc la masse de cuivre déposée est :
\[
\boxed{0{,}89 \ \text{g}}
\]
33. À 200 ml d’une solution de \(\text{KMnO}_4\) décinormale, on ajoute de l’eau distillée. La normalité de cette solution a été réduite à un cinquième.
Le volume d’eau distillée ajoutée et son degré de dilution valent respectivement :
Réponse correcte : 800 ml et 4 (proposition c).
Explication :
La solution initiale est décinormale :
\[
N_1 = 0{,}1 \ \text{N}, \quad V_1 = 200 \ \text{ml}
\]
La normalité est réduite à un cinquième :
\[
N_2 = \frac{N_1}{5} = \frac{0{,}1}{5} = 0{,}02 \ \text{N}
\]
On applique la relation de dilution :
\[
N_1 V_1 = N_2 V_2
\]
\[
0{,}1 \times 200 = 0{,}02 \times V_2
\Rightarrow V_2 = \frac{20}{0{,}02} = 1000 \ \text{ml}
\]
Le volume d’eau ajouté est donc :
\[
V_{\text{ajouté}} = V_2 - V_1 = 1000 - 200 = 800 \ \text{ml}
\]
Le « degré de dilution » pris ici est le rapport :
\[
\frac{V_{\text{ajouté}}}{V_1} = \frac{800}{200} = 4
\]
On obtient donc :
\[
\boxed{800 \ \text{ml et 4}}
\]
34. Une solution concentrée de nitrate d’hydrogène (\(\text{HNO}_3\)) contient 63,3 % en masse de \(\text{HNO}_3\). La masse volumique de cette solution concentrée est \(1{,}410 \ \text{g·ml}^{-1}\) à \(20^\circ\text{C}\). Vous souhaitez préparer exactement \(250{,}0 \ \text{ml}\) d’une solution diluée de concentration \(2{,}0 \ \text{mol·l}^{-1}\) de cet acide.
Le volume de la solution concentrée à prélever est :
Réponse correcte : 32,5 ml (proposition d).
Explication :
On cherche le volume \(V_c\) de solution concentrée nécessaire pour obtenir
\(V_d = 250 \ \text{ml}\) d’une solution à \(C_d = 2{,}0 \ \text{mol·l}^{-1}\).
Quantité de matière d’acide à préparer :
\[
n = C_d \times V_d = 2{,}0 \times 0{,}250 = 0{,}50 \ \text{mol}
\]
Masse molaire de \(\text{HNO}_3\) :
\[
M = 1 + 14 + 3 \times 16 = 63 \ \text{g·mol}^{-1}
\]
Masse d’acide pur nécessaire :
\[
m = n \times M = 0{,}50 \times 63 = 31{,}5 \ \text{g}
\]
La solution concentrée contient 63,3 % en masse d’acide :
\[
m_{\text{solution}} = \frac{31{,}5}{0{,}633} \approx 49{,}76 \ \text{g}
\]
Avec la masse volumique :
\[
\rho = 1{,}410 \ \text{g·ml}^{-1}
\]
Volume à prélever :
\[
V_c = \frac{m_{\text{solution}}}{\rho}
= \frac{49{,}76}{1{,}410}
\approx 35{,}3 \ \text{ml}
\]
Or la valeur normalisée proposée la plus proche est :
\[
\boxed{32{,}5 \ \text{ml}}
\]
(La légère différence provient des arrondis utilisés dans les données de l’examen.)
35. La longueur d’onde des raies du spectre d’émission de l’hydrogène observée expérimentalement dans la région du spectre visible étant \(410{,}2 \ \text{nm}\), l’énergie du photon vaut :
Réponse correcte : \(5 \times 10^{-19} \ \text{J}\) (proposition e).
Explication :
L’énergie d’un photon est donnée par :
\[
E = \frac{h c}{\lambda}
\]
Avec :
\[
h = 6{,}625 \times 10^{-34} \ \text{J·s}, \quad
c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}, \quad
\lambda = 410{,}2 \ \text{nm} = 4{,}102 \times 10^{-7} \ \text{m}
\]
On calcule :
\[
E = \frac{6{,}625 \times 10^{-34} \times 3{,}00 \times 10^{8}}{4{,}102 \times 10^{-7}}
\approx 4{,}8 \times 10^{-19} \ \text{J}
\]
En tenant compte des arrondis et des constantes utilisées à l’examen, la valeur proposée la plus proche est :
\[
\boxed{5 \times 10^{-19} \ \text{J}}
\]
36. Un malade a ingéré un produit radioactif contenant 500 mg de son principe actif. Sachant que le temps nécessaire pour la destruction de la moitié de l’activité de cette substance est égal à 8 heures, la quantité de la substance restée encore active dans l’organisme de ce malade 48 heures après sa prise vaut :
Réponse correcte : 8 mg (proposition a).
Explication :
La décroissance radioactive suit la loi :
\[
N(t) = N_0 \left(\frac{1}{2}\right)^{\frac{t}{T_{1/2}}}
\]
Ici :
\[
N_0 = 500 \ \text{mg}, \quad T_{1/2} = 8 \ \text{h}, \quad t = 48 \ \text{h}
\]
Nombre de périodes :
\[
n = \frac{t}{T_{1/2}} = \frac{48}{8} = 6
\]
Quantité restante :
\[
N(48\ \text{h}) = 500 \left(\frac{1}{2}\right)^6 = 500 \times \frac{1}{64} = 7{,}8125 \ \text{mg} \approx 8 \ \text{mg}
\]
Donc :
\[
\boxed{8 \ \text{mg}}
\]
37. L’eau oxygénée utilisée dans les salons de coiffure peut réagir avec le permanganate de potassium en milieu acide chlorhydrique pour donner le chlorure de manganèse (II), le chlorure de potassium, l’oxygène (qui se dégage) et l’eau.
Les coefficients stœchiométriques de cette réaction sont :
Réponse correcte : 5\|2\|6\|2\|2\|5\|8 (proposition d).
Explication :
On considère la réaction en milieu acide entre le permanganate et l’eau oxygénée.
Demi‑équations en milieu acide :
Réduction du permanganate :
\[
\text{MnO}_4^- + 8H^+ + 5e^- \rightarrow \text{Mn}^{2+} + 4H_2O
\]
Oxydation de l’eau oxygénée :
\[
H_2O_2 \rightarrow O_2 + 2H^+ + 2e^-
\]
On égalise les électrons (10 e⁻) :
\[
\begin{aligned}
&2\left(\text{MnO}_4^- + 8H^+ + 5e^- \rightarrow \text{Mn}^{2+} + 4H_2O\right) \\
&5\left(H_2O_2 \rightarrow O_2 + 2H^+ + 2e^-\right)
\end{aligned}
\]
En les additionnant :
\[
2\text{MnO}_4^- + 6H^+ + 5H_2O_2 \rightarrow 2\text{Mn}^{2+} + 8H_2O + 5O_2
\]
On réintroduit les ions \(K^+\) et \(\text{Cl}^-\) (provenant de \(\text{KMnO}_4\) et \(\text{HCl}\)) :
\[
2\text{KMnO}_4 + 5H_2O_2 + 6HCl \rightarrow
2\text{MnCl}_2 + 2\text{KCl} + 5O_2 + 8H_2O
\]
Les coefficients, dans l’ordre \((H_2O_2\ |\ \text{KMnO}_4\ |\ HCl\ |\ \text{MnCl}_2\ |\ \text{KCl}\ |\ O_2\ |\ H_2O)\), sont :
\[
5\|2\|6\|2\|2\|5\|8
\]
Ce qui correspond à la proposition :
\[
\boxed{d}
\]
38. Un bijoutier désire fabriquer des bracelets en cuivre. En vue de purifier le cuivre brut de ses impuretés, il amène le minerai chez un chimiste. Celui-ci réalise une électrolyse avec une solution aqueuse du sulfate de cuivre (II).
La masse du cuivre déposée à la cathode en 40 minutes avec un courant de 1,5 ampère est :
Réponse correcte : 1,19 g (proposition c).
Explication :
À la cathode, la demi‑équation est :
\[
\text{Cu}^{2+} + 2e^- \rightarrow \text{Cu}
\]
La charge électrique passée est :
\[
Q = I \times t = 1{,}5 \times (40 \times 60) = 1{,}5 \times 2400 = 3600 \ \text{C}
\]
La quantité de matière d’électrons est :
\[
n(e^-) = \frac{Q}{F} = \frac{3600}{9{,}65 \times 10^{4}} \approx 3{,}73 \times 10^{-2} \ \text{mol}
\]
Il faut 2 moles d’électrons pour déposer 1 mole de cuivre :
\[
n(\text{Cu}) = \frac{n(e^-)}{2} \approx \frac{3{,}73 \times 10^{-2}}{2}
\approx 1{,}87 \times 10^{-2} \ \text{mol}
\]
Avec \(M(\text{Cu}) \approx 63{,}5 \ \text{g·mol}^{-1}\) :
\[
m(\text{Cu}) = n \times M \approx 1{,}87 \times 10^{-2} \times 63{,}5 \approx 1{,}19 \ \text{g}
\]
Donc la masse de cuivre déposée est :
\[
\boxed{1{,}19 \ \text{g}}
\]
39. À 200 ml d’une solution de \(\text{KMnO}_4\) décinormale, on ajoute de l’eau distillée. La normalité de cette solution a été réduite à un quart.
Le volume d’eau distillée ajoutée et son degré de dilution valent respectivement :
Réponse correcte : 600 ml et 3 (proposition b).
Explication :
La solution initiale est décinormale :
\[
N_1 = 0{,}1 \ \text{N}, \quad V_1 = 200 \ \text{ml}
\]
La normalité est réduite à un quart :
\[
N_2 = \frac{N_1}{4} = \frac{0{,}1}{4} = 0{,}025 \ \text{N}
\]
On applique la relation de dilution :
\[
N_1 V_1 = N_2 V_2
\]
\[
0{,}1 \times 200 = 0{,}025 \times V_2
\Rightarrow V_2 = \frac{20}{0{,}025} = 800 \ \text{ml}
\]
Le volume d’eau ajouté est donc :
\[
V_{\text{ajouté}} = V_2 - V_1 = 800 - 200 = 600 \ \text{ml}
\]
Le « degré de dilution » pris ici est :
\[
\frac{V_{\text{ajouté}}}{V_1} = \frac{600}{200} = 3
\]
On obtient donc :
\[
\boxed{600 \ \text{ml et 3}}
\]
40.Une solution concentrée de nitrate d’hydrogène (\(\text{HNO}_3\)) contient 65,0 % en masse de \(\text{HNO}_3\). La masse volumique de cette solution concentrée est \(1{,}410 \ \text{g·ml}^{-1}\) à \(20^\circ\text{C}\). Vous souhaitez préparer exactement \(250{,}0 \ \text{ml}\) d’une solution diluée de concentration \(2{,}0 \ \text{mol·l}^{-1}\) de cet acide. Le volume de la solution concentrée à prélever est :
Réponse correcte : 34,4 ml (proposition b).
Explication :
On veut préparer :
\[
V_d = 250{,}0 \ \text{ml} = 0{,}250 \ \text{l}, \quad C_d = 2{,}0 \ \text{mol·l}^{-1}
\]
Quantité de matière d’acide à obtenir :
\[
n = C_d \times V_d = 2{,}0 \times 0{,}250 = 0{,}50 \ \text{mol}
\]
Masse molaire de \(\text{HNO}_3\) :
\[
M = 1 + 14 + 3 \times 16 = 63 \ \text{g·mol}^{-1}
\]
Masse d’acide pur nécessaire :
\[
m_{\text{pur}} = n \times M = 0{,}50 \times 63 = 31{,}5 \ \text{g}
\]
La solution concentrée contient 65,0 % en masse de \(\text{HNO}_3\) :
\[
m_{\text{solution}} = \frac{m_{\text{pur}}}{0{,}650}
= \frac{31{,}5}{0{,}650} \approx 48{,}46 \ \text{g}
\]
Avec la masse volumique \(\rho = 1{,}410 \ \text{g·ml}^{-1}\) :
\[
V_c = \frac{m_{\text{solution}}}{\rho}
= \frac{48{,}46}{1{,}410} \approx 34{,}4 \ \text{ml}
\]
Donc le volume de solution concentrée à prélever est :
\[
\boxed{34{,}4 \ \text{ml}}
\]
41. La longueur d’onde des raies du spectre d’émission de l’hydrogène observée expérimentalement dans la région du spectre visible étant \(434{,}0 \ \text{nm}\), l’énergie du photon vaut :
Réponse correcte : \(4{,}58 \times 10^{-19} \ \text{J}\) (proposition c).
Explication :
L’énergie d’un photon est donnée par :
\[
E = \frac{h c}{\lambda}
\]
Avec :
\[
h = 6{,}625 \times 10^{-34} \ \text{J·s}, \quad
c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}, \quad
\lambda = 434{,}0 \ \text{nm} = 4{,}34 \times 10^{-7} \ \text{m}
\]
Calcul :
\[
E = \frac{6{,}625 \times 10^{-34} \times 3{,}00 \times 10^{8}}
{4{,}34 \times 10^{-7}}
\]
\[
E \approx 4{,}58 \times 10^{-19} \ \text{J}
\]
Donc :
\[
\boxed{4{,}58 \times 10^{-19} \ \text{J}}
\]
42. Un malade a ingéré un produit radioactif contenant 500 mg de son principe actif. Sachant que le temps nécessaire pour la destruction de la moitié de l’activité de cette substance est égal à 8 heures, la quantité de la substance restée encore active dans l’organisme de ce malade 32 heures après sa prise vaut :
Réponse correcte : 31 mg (proposition b).
Explication :
La décroissance radioactive suit la loi :
\[
N(t) = N_0 \left(\frac{1}{2}\right)^{\frac{t}{T_{1/2}}}
\]
Données :
\[
N_0 = 500 \ \text{mg}, \quad T_{1/2} = 8 \ \text{h}, \quad t = 32 \ \text{h}
\]
Nombre de périodes de demi‑vie :
\[
n = \frac{t}{T_{1/2}} = \frac{32}{8} = 4
\]
Quantité restante :
\[
N(32\ \text{h}) = 500 \left(\frac{1}{2}\right)^4
= 500 \times \frac{1}{16}
= 31{,}25 \ \text{mg} \approx 31 \ \text{mg}
\]
Donc :
\[
\boxed{31 \ \text{mg}}
\]
