Exetat Chimie 2025_Scientifique
1. Un échantillon de NaI est injecté à un patient dans le cadre du traitement d’un cancer de la thyroïde. Si l’échantillon a une radioactivité de 10,000 dés/min à 8h50’, sachant que sa période radioactive ou demi-vie est de 25 minutes. Sa radioactivité (en dés/min) à 10h05’ sera :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Correction accessible uniquement après paiement.
Payer pour voir la correction
2. Pendant le tour de salles dans un centre de santé, le médecin prescrit pour un octogénaire \(2 \times 10^{21}\) molécules de l’acide acétylsalicylique ou aspirine \(\text{C}_9\text{H}_8\text{O}_4\). La masse de ce médicament (en mg) est :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Correction accessible uniquement après paiement.
Payer pour voir la correction
3. Dans un laboratoire d’une usine de fabrication des médicaments, il est demandé de diluer deux fois une solution molaire obtenue par dissolution de 52,8 g d’acide ascorbique (ou vitamine C), de formule ci‑contre. Le volume (en litre) de la solution diluée vaut : 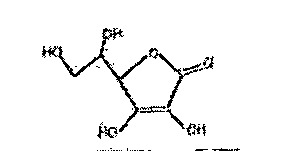
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32
Correction accessible uniquement après paiement.
Payer pour voir la correction
4. Voici ci‑contre le schéma de l’électrolyse de l’eau pour produire principalement de l’hydrogène gazeux.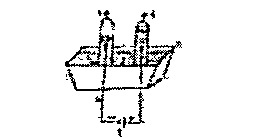
Le chiffre 3 désigne :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32
Correction accessible uniquement après paiement.
Payer pour voir la correction
5. En vue d’une analyse au laboratoire, un chimiste pèse 2,2 g de soude caustique. Il ajoute de l’eau distillée et une goutte d’un indicateur coloré. La neutralisation s’obtient par adjonction de 60 ml d’une solution de l’acide sulfurique 0,3 M. Le pourcentage NaOH contenu dans cette solution est :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Correction accessible uniquement après paiement.
Payer pour voir la correction
6. 6. Lors de la réaction d’oxydo‑réduction, l’acide sulfurique concentré et chaud est un agent oxydant vis‑à‑vis du mercure. On obtient des ions mercuriques et un dégagement de dioxyde de soufre. La masse de mercure à utiliser pour obtenir 3 litres de dioxyde de soufre gazeux dans les conditions normales vaut :
Réaction chimique : \(\text{Hg} + \text{H}_2\text{SO}_4 \rightarrow \text{HgSO}_4 + \text{SO}_2 + \text{H}_2\text{O}\).
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Correction accessible uniquement après paiement.
Payer pour voir la correction
7. Un échantillon de NaI est injecté à un patient dans le cadre du traitement d’un cancer de la thyroïde. Si l’échantillon a une radioactivité de 10000 dés/min à 10h05’, sachant que sa période radioactive ou demi-vie est de 25 minutes. Sa radioactivité (en dés/min) à 11h45’ sera :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Correction accessible uniquement après paiement.
Payer pour voir la correction
8. Dans un laboratoire d’une usine de fabrication des médicaments, il est demandé de diluer deux fois une solution molaire obtenue par dissolution de 70,4 g d’acide ascorbique (ou vitamine C), de formule ci‑contre.
Le volume (en litre) de la solution diluée vaut :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Correction accessible uniquement après paiement.
Payer pour voir la correction
9. Voici ci‑contre le schéma de l’électrolyse de l’eau pour produire principalement de l’hydrogène gazeux.
Le chiffre 2 désigne :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Correction accessible uniquement après paiement.
Payer pour voir la correction
10. En vue d’une analyse au laboratoire, un chimiste pèse 2,5 g de soude caustique. Il ajoute de l’eau distillée et une goutte d’un indicateur coloré. La neutralisation s’obtient par adjonction de 60 ml d’une solution de l’acide sulfurique 0,3 M. Le pourcentage NaOH contenu dans cette solution est :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Correction accessible uniquement après paiement.
Payer pour voir la correction
Lors de la réaction d’oxydo‑réduction, l’acide sulfurique concentré et chaud est un agent oxydant vis‑à‑vis du mercure. On obtient des ions mercuriques et un dégagement de dioxyde de soufre. La masse de mercure à utiliser pour obtenir 4 litres de dioxyde de soufre gazeux dans les conditions normales vaut :Réaction chimique : \(\text{Hg} + \text{H}_2\text{SO}_4 \rightarrow \text{HgSO}_4 + \text{SO}_2 + \text{H}_2\text{O}\).
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Correction accessible uniquement après paiement.
Payer pour voir la correction
12. Pendant le tour de salles dans un centre de santé, le médecin prescrit pour un adolescent \(1{,}5 \times 10^{21}\) molécules de l’acide acétylsalicylique ou aspirine \(\text{C}_9\text{H}_8\text{O}_4\). La masse de ce médicament (en mg) est :
Données communes Masse atomique : C = 12 ; Ca = 40 ; H = 1 ; O = 16 ; N = 14 ; Hg = 200,59 ; S = 32.
Correction accessible uniquement après paiement.
Payer pour voir la correction
13. Lors de la fabrication des engrais chimiques dans une industrie, un chimiste prépare 9 l d’acide sulfurique 0,1 N. Le volume de l’acide sulfurique concentré (95 % et masse volumique 1,8 g/ml) qu’il faut diluer est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
14.Un chasseur a retrouvé dans une forêt le crâne d’un homme dont la quantité de carbone‑14 est 4 fois moins que celle rencontrée dans une personne vivante.
L’âge approximatif de l’être humain ayant vécu dans cette forêt est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
15. Un volume de 1,0 l d’une solution d’eau oxygénée produit, lors de sa décomposition spontanée, 110 l de dioxygène sous une pression de 1,0 bar et à une température de 0 °C.
Réaction : \(\text{H}_2\text{O}_2 \rightarrow \text{H}_2\text{O} + \tfrac{1}{2}\text{O}_2\)
La quantité de dioxygène produite lors de la décomposition de \(V_0 = 0,16\) l de cette solution d’eau oxygénée est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
16. Selon la loi de Faraday en électrolyse : « La quantité des substances obtenues aux électrodes est proportionnelle à la quantité de courant utilisé ».
La masse de zinc déposée en 2 heures à la cathode d’un voltamètre à sulfate de zinc lorsqu’il est traversé par un courant de 0,5 A est égale à :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
17. Lors d’un dosage de 10 ml de \(\text{H}_2\text{SO}_4\) 0,1 N par une solution de \(\text{Ca(OH)}_2\) 0,1 N, après avoir laissé couler goutte à goutte un volume précis de la base, la masse du sel formé est de 0,034 g.
Le volume de la solution basique correspondant à cette masse est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
18. Un chimiste reçoit quatre bouteilles d’un litre de solution d’acide de batterie (\(\text{H}_2\text{SO}_4\)). Voulant connaître la masse de l’acide pur contenu dans chaque bouteille, il prélève 50 ml de chaque bouteille et les titre par une solution de \(\text{NaOH}\). Il sort du laboratoire avec les graphiques ci‑dessous.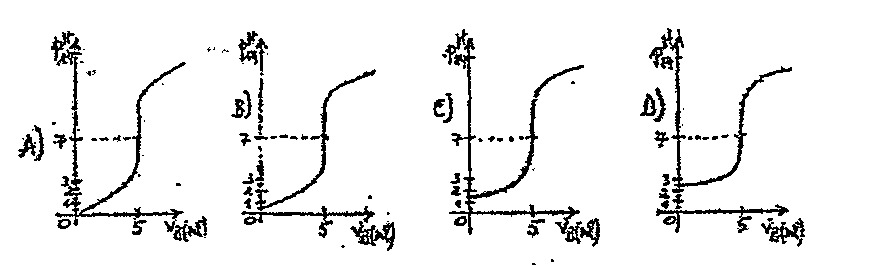
Après analyse et interprétation de ces graphiques, la masse en gramme de l’acide contenu dans la solution utilisée au graphique B vaut :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
19. Lors de la fabrication des engrais chimiques dans une industrie, un chimiste prépare 8 l d’acide sulfurique 0,1 N.
Le volume de l’acide sulfurique concentré (95 % et masse volumique 1,8 g/ml) qu’il faut diluer est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
20. Un chasseur a retrouvé dans une forêt le crâne d’un homme dont la quantité de carbone‑14 est 6 fois moins que celle rencontrée dans une personne vivante.
L’âge approximatif de l’être humain ayant vécu dans cette forêt est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
21.Un volume de 1,0 l d’une solution d’eau oxygénée produit, lors de sa décomposition spontanée, 110 l de dioxygène sous une pression de 1,0 bar et à une température de 0 °C.
Réaction : \(\text{H}_2\text{O}_2 \rightarrow \text{H}_2\text{O} + \tfrac{1}{2}\text{O}_2\).
La quantité de dioxygène produite lors de la décomposition de \(V_0 = 0,17\) l de cette solution d’eau oxygénée est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
22. Selon la loi de Faraday en électrolyse : « La quantité des substances obtenues aux électrodes est proportionnelle à la quantité de courant utilisé ».
La masse de zinc déposée en 2 heures à la cathode d’un voltamètre à sulfate de zinc lorsqu’il est traversé par un courant de 0,6 A est égale à :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
23. Lors d’un dosage de 10 ml de \(\text{H}_2\text{SO}_4\) 0,1 N par une solution de \(\text{Ca(OH)}_2\) 0,1 N, après avoir laissé couler goutte à goutte un volume précis de la base, la masse du sel formé est de 0,054 g.
Le volume de la solution basique correspondant à cette masse est :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
24. Un chimiste reçoit quatre bouteilles d’un litre de solution d’acide de batterie (\(\text{H}_2\text{SO}_4\)). Voulant connaître la masse de l’acide pur contenu dans chaque bouteille, il prélève 50 ml de chaque bouteille et les titre par une solution de \(\text{NaOH}\). Il sort du laboratoire avec les graphiques ci‑dessous.
Après analyse et interprétation de ces graphiques, la masse en gramme de l’acide contenue dans la solution utilisée au graphique A vaut :
Données :
\(R = 8{,}314 \ \text{J·mol}^{-1}\text{·K}^{-1}\)
\(F = 9{,}65 \times 10^{4} \ \text{C·mol}^{-1}\)
Constante d’Avogadro : \(6{,}02 \times 10^{23} \ \text{mol}^{-1}\)
Masses atomiques : Zinc = 65,4 ;H = 1; O = 16 ;S = 32; Ca = 40 ; C = 12
Valeurs approchées : \(10^{0,3} = 2\) ; \(10^{0,4} = 2{,}5\) -;\(10^{0,5} = 3\)
Période du Carbone‑14 : \(5700 \ \text{ans}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
25.100 ml d’un vin contenant 9,0 ml d’éthanol de masse volumique \(\rho = 790 \ \text{kg·m}^{-3}\), abandonné à l’air, s’oxyde et se transforme en vinaigre selon l’équation chimique ci‑après : \[ \text{CH}_3\text{CH}_2\text{OH} + \text{O}_2 \rightarrow \text{CH}_3\text{COOH} + \text{H}_2\text{O} \] La masse maximale d’acide formée lors de la transformation d’un litre de vin à 10^\circ\text{C} vaut :
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
26. En médecine, les atomes radioactifs sont utilisés comme source de rayonnement.
Parmi les éléments ci‑dessous, lesquels déterminent le volume du sang que contient le corps humain.
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
27. Soit le spectre de la lumière :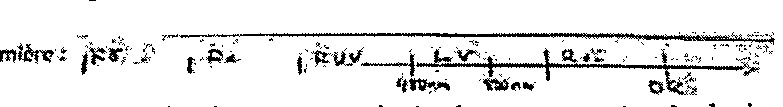
La lumière est constituée des composantes à plusieurs longueurs d’onde (\(\lambda\)) allant du rayon gamma (\(\gamma\)) jusqu’aux ondes radio (OR).
L’énergie de liaison simple C–C dans le composé \(\text{C}_6\text{H}_6 (g)\) est égale à \(345 \ \text{kJ·mol}^{-1}\).
La longueur d’onde de la lumière capable de transformer l’éthane en méthane selon cette équation chimique :
\[ \text{C}_2\text{H}_6 (g) \rightarrow 2 \text{CH}_4 \]
vaut… et est située dans :
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
28. On dissout 0,532 g de \(\text{IO}_3\), sel oxydant, dans l’eau distillée pour obtenir 300 ml de solution. Sachant que le couple oxydo‑réducteur est \(\text{IO}_3^-/\text{I}_2\).
La normalité de la solution préparée est :
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
29. Au laboratoire de l’ITA/Mombele, Paul fait réagir 300 ml de l’acide benzoïque \(0{,}5 \ \text{mol·l}^{-1} \ (C_6H_5CO_2H), \ pK_a = 4{,}2\) avec 700 ml d’une solution d’hydroxyde de sodium décimolaire.
Le \(pH\) du mélange vaut :
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
30. Au laboratoire, lors de la saponification, on prépare 20 ml d’une solution de soude caustique 0,2 N. On y ajoute 40 ml d’eau.
La concentration de la nouvelle solution est :
Données :
Masses atomiques : \(\text{C} = 12\) ; \(\text{O} = 16\) ; \(\text{H} = 1\) ; \(\text{K} = 39\) ; \(\text{I} = 127\) ; \(\text{Na} = 23\)
Constantes physiques : \(h = 6{,}625 \times 10^{-34} \ \text{J·s}\) ; \(c = 3{,}00 \times 10^{8} \ \text{m·s}^{-1}\) ; \(N_A = 6{,}022 \times 10^{23} \ \text{mol}^{-1}\)
Correction accessible uniquement après paiement.
Payer pour voir la correction
31. Le permanganate de potassium réagit avec le bromure de potassium en milieu acide sulfurique pour donner le sulfate de manganèse (II), le sulfate de potassium, le brome et l’eau.
Les coefficients stœchiométriques de cette réaction sont :
Correction accessible uniquement après paiement.
Payer pour voir la correction
32. Un bijoutier désire fabriquer des bracelets en cuivre. En vue de purifier le cuivre brut de ses impuretés, il amène le minerai chez un chimiste. Celui-ci réalise une électrolyse avec une solution aqueuse du sulfate de cuivre (II). La masse du cuivre déposée à la cathode en 30 minutes avec un courant de 1,5 ampère est :
Correction accessible uniquement après paiement.
Payer pour voir la correction
33. À 200 ml d’une solution de \(\text{KMnO}_4\) décinormale, on ajoute de l’eau distillée. La normalité de cette solution a été réduite à un cinquième.
Le volume d’eau distillée ajoutée et son degré de dilution valent respectivement :
Correction accessible uniquement après paiement.
Payer pour voir la correction
34. Une solution concentrée de nitrate d’hydrogène (\(\text{HNO}_3\)) contient 63,3 % en masse de \(\text{HNO}_3\). La masse volumique de cette solution concentrée est \(1{,}410 \ \text{g·ml}^{-1}\) à \(20^\circ\text{C}\). Vous souhaitez préparer exactement \(250{,}0 \ \text{ml}\) d’une solution diluée de concentration \(2{,}0 \ \text{mol·l}^{-1}\) de cet acide.
Le volume de la solution concentrée à prélever est :
Correction accessible uniquement après paiement.
Payer pour voir la correction
35. La longueur d’onde des raies du spectre d’émission de l’hydrogène observée expérimentalement dans la région du spectre visible étant \(410{,}2 \ \text{nm}\), l’énergie du photon vaut :
Correction accessible uniquement après paiement.
Payer pour voir la correction
36. Un malade a ingéré un produit radioactif contenant 500 mg de son principe actif. Sachant que le temps nécessaire pour la destruction de la moitié de l’activité de cette substance est égal à 8 heures, la quantité de la substance restée encore active dans l’organisme de ce malade 48 heures après sa prise vaut :
Correction accessible uniquement après paiement.
Payer pour voir la correction
37. L’eau oxygénée utilisée dans les salons de coiffure peut réagir avec le permanganate de potassium en milieu acide chlorhydrique pour donner le chlorure de manganèse (II), le chlorure de potassium, l’oxygène (qui se dégage) et l’eau.
Les coefficients stœchiométriques de cette réaction sont :
Correction accessible uniquement après paiement.
Payer pour voir la correction
38. Un bijoutier désire fabriquer des bracelets en cuivre. En vue de purifier le cuivre brut de ses impuretés, il amène le minerai chez un chimiste. Celui-ci réalise une électrolyse avec une solution aqueuse du sulfate de cuivre (II).
La masse du cuivre déposée à la cathode en 40 minutes avec un courant de 1,5 ampère est :
Correction accessible uniquement après paiement.
Payer pour voir la correction
39. À 200 ml d’une solution de \(\text{KMnO}_4\) décinormale, on ajoute de l’eau distillée. La normalité de cette solution a été réduite à un quart.
Le volume d’eau distillée ajoutée et son degré de dilution valent respectivement :
Correction accessible uniquement après paiement.
Payer pour voir la correction
40.Une solution concentrée de nitrate d’hydrogène (\(\text{HNO}_3\)) contient 65,0 % en masse de \(\text{HNO}_3\). La masse volumique de cette solution concentrée est \(1{,}410 \ \text{g·ml}^{-1}\) à \(20^\circ\text{C}\). Vous souhaitez préparer exactement \(250{,}0 \ \text{ml}\) d’une solution diluée de concentration \(2{,}0 \ \text{mol·l}^{-1}\) de cet acide. Le volume de la solution concentrée à prélever est :
Correction accessible uniquement après paiement.
Payer pour voir la correction
41. La longueur d’onde des raies du spectre d’émission de l’hydrogène observée expérimentalement dans la région du spectre visible étant \(434{,}0 \ \text{nm}\), l’énergie du photon vaut :
Correction accessible uniquement après paiement.
Payer pour voir la correction
42. Un malade a ingéré un produit radioactif contenant 500 mg de son principe actif. Sachant que le temps nécessaire pour la destruction de la moitié de l’activité de cette substance est égal à 8 heures, la quantité de la substance restée encore active dans l’organisme de ce malade 32 heures après sa prise vaut :
Correction accessible uniquement après paiement.
Payer pour voir la correction