Exetat Chimie 2024_Scientifique
Question 1
1. Un chimiste titre 20 ml d’une solution de jus de citron par une solution normale d’hydroxyde de sodium en présence de phénolphtaléine. Du laboratoire, il obtient la courbe suivante représentant l’évolution du pH en fonction du volume \(V_B\) de base ajoutée.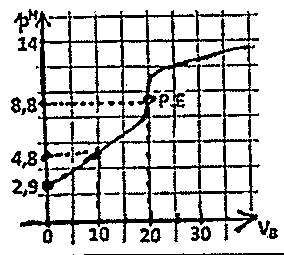
Le \(pH\) de la solution obtenue après addition de 5 ml de base est :
Réponse correcte : 4,7 (proposition a).
Explication :
On lit la valeur du pH directement sur la courbe de titrage.
Pour un volume de base ajouté \(V_B = 5 \ \text{ml}\), le point correspondant sur la courbe
se situe dans la zone acide, entre les valeurs de pH marquées 2,9 et 4,8, très proche de 4,7.
Par interpolation graphique, on obtient donc :
\[
pH \approx 4{,}7
\]
Ce qui correspond à la proposition :
\[
\boxed{4{,}7}
\]
2. Les radioisotopes sont des noyaux atomiques très dangereux à cause des radiations nocives qu’ils émettent. À des quantités très contrôlées, ces radioisotopes sont utilisés en chimiothérapie. Pour diagnostiquer ou localiser les tumeurs de cerveau, la médecine utilise :
Réponse correcte : le technétium – 99 (proposition e).
Explication :
Le \(\text{technétium–99m}\) (forme métastable du technétium–99) est largement utilisé en médecine
nucléaire comme traceur pour l’imagerie (scintigraphie), notamment pour l’exploration du cerveau.
Il émet des rayonnements \(\gamma\) facilement détectables, avec une période relativement courte,
ce qui limite la dose reçue par le patient tout en donnant une image précise de la zone à explorer.
Les autres radioisotopes ont d’autres usages principaux :
iode–131 pour la thyroïde, cobalt–60 pour la radiothérapie, sodium–24 pour l’étude de la circulation sanguine, etc.
Ainsi, pour localiser les tumeurs cérébrales, on utilise :
\[
\boxed{\text{le technétium – 99}}
\]
3. Les diététiciens recommandent actuellement l’eau comme un médicament en raison de 40 ml par kilogramme de masse corporelle, par jour. Sachant qu’une eau potable doit contenir 80 mg de calcaire, le nombre d’atomes de calcium qu’un enfant pesant 62,5 kg doit consommer journalièrement est égal à :
Réponse correcte : \(120 \times 10^{19}\) (proposition e).
Explication :
Volume d’eau recommandé par jour :
\[
V = 40 \ \text{ml·kg}^{-1} \times 62{,}5 \ \text{kg} = 2500 \ \text{ml} = 2{,}5 \ \text{l}
\]
Chaque litre contient 80 mg de calcaire (assimilé à \(\text{CaCO}_3\)) :
\[
m = 2{,}5 \times 80 \ \text{mg} = 200 \ \text{mg} = 0{,}200 \ \text{g}
\]
Masse molaire de \(\text{CaCO}_3 \approx 100 \ \text{g·mol}^{-1}\) :
\[
n(\text{CaCO}_3) = \frac{0{,}200}{100} = 2{,}0 \times 10^{-3} \ \text{mol}
\]
Chaque mole de \(\text{CaCO}_3\) contient 1 mole d’atomes de calcium :
\[
n(\text{Ca}) = 2{,}0 \times 10^{-3} \ \text{mol}
\]
Nombre d’atomes de calcium :
\[
N = n \times N_A = 2{,}0 \times 10^{-3} \times 6{,}02 \times 10^{23}
\approx 1{,}20 \times 10^{21} = 120 \times 10^{19}
\]
Donc :
\[
\boxed{120 \times 10^{19}}
\]
4. Une analysticienne fait réagir 30 g d’un échantillon de sel de cuisine avec une solution de nitrate d’argent et précipite le chlorure d’argent qui, après filtration, lavage et séchage, pèse 50,0 g. La teneur (en %) de chlore dans l’échantillon vaut :
Réponse correcte : 41 % (proposition c).
Explication :
Le précipité formé est le chlorure d’argent \(\text{AgCl}\).
Masse molaire :
\[
M(\text{AgCl}) = M(\text{Ag}) + M(\text{Cl}) \approx 108{,}0 + 35{,}5 = 143{,}5 \ \text{g·mol}^{-1}
\]
Dans 1 mole de \(\text{AgCl}\), la masse de chlore est 35,5 g.
Dans 50,0 g de \(\text{AgCl}\), la masse de chlore vaut donc :
\[
m_{\text{Cl}} = 50{,}0 \times \frac{35{,}5}{143{,}5} \approx 12{,}4 \ \text{g}
\]
Cette masse de chlore provient des 30 g de l’échantillon de sel de cuisine.
La teneur massique en chlore est alors :
\[
\%\text{Cl} = \frac{12{,}4}{30} \times 100 \approx 41{,}3 \ \% \approx 41 \ \%
\]
Donc :
\[
\boxed{41 \ \%}
\]
5. Un électrochimiste réalise une pile galvanique représentée par le schéma : \[ \text{Zn} \, | \, \text{Zn}^{2+} \, \| \, \text{Cu}^{2+} \, | \, \text{Cu} \] avec : \[ E^\circ(\text{Zn}^{2+}/\text{Zn}) = -0{,}76 \ \text{V} \quad ; \quad E^\circ(\text{Cu}^{2+}/\text{Cu}) = +0{,}34 \ \text{V} \]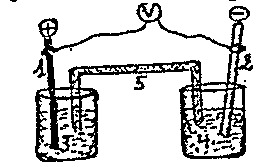
Après analyse et interprétation de ce croquis, le chiffre 4 présente :
Réponse correcte : \(K_{2}SO_{4}(aq)\) (proposition c).
Explication :
La pile \(\text{Zn} \, | \, \text{Zn}^{2+} \, \| \, \text{Cu}^{2+} \, | \, \text{Cu}\) est constituée :
- d’une électrode de zinc plongée dans une solution contenant \(\text{Zn}^{2+}\),
- d’une électrode de cuivre plongée dans une solution contenant \(\text{Cu}^{2+}\),
- d’un pont salin reliant les deux solutions.
Le pont salin contient un électrolyte inerte (qui ne réagit pas avec les espèces de la pile), typiquement une solution de \(\text{K}_{2}\text{SO}_{4}(aq)\) ou de \(\text{KNO}_{3}(aq)\), permettant la circulation des ions pour assurer l’électroneutralité.
Sur le croquis, le chiffre 4 désigne précisément ce pont salin et donc la solution de l’électrolyte inerte :
\[
\boxed{K_{2}SO_{4}(aq)}
\]
6. Les feux d’artifice émettent une incandescence multicolore dont la radiation rouge a une longueur d’onde égale à 900 nm. L’énergie libérée par cette radiation pyrotechnique vaut (en Mev) :
Réponse Correcte : a. \(1381 \cdot 10^{12}\)
Explication :
1. Formule de base :
L'énergie \(\mathrm{E}\) d'un photon est calculée par la relation de Planck :
\(\mathrm{E = \frac{h \cdot c}{\lambda}}\)
Où :
* \(\mathrm{h}\) (constante de Planck) \(\approx 6,62 \cdot 10^{-34}\ \mathrm{J \cdot s}\)
* \(\mathrm{c}\) (vitesse de la lumière) \(\approx 3 \cdot 10^{8}\ \mathrm{m/s}\)
* \(\lambda\) (longueur d'onde) \(= 900\ \mathrm{nm} = 900 \cdot 10^{-9}\ \mathrm{m}\)
2. Calcul en Joules (\(\mathrm{J}\)) :
\(\mathrm{E = \frac{6,62 \cdot 10^{-34} \cdot 3 \cdot 10^{8}}{900 \cdot 10^{-9}}}\)
\(\mathrm{E \approx 2,2 \cdot 10^{-19}\ J}\)
3. Conversion en MeV (Mega-électronvolt) :
Pour obtenir l'énergie totale par mole de photons (ce qui correspond aux puissances de \(10^{12}\) des assertions) :
* On multiplie par le nombre d'Avogadro \(\mathrm{N_A = 6,02 \cdot 10^{23}}\).
* On convertit les Joules en eV (\(1\ \mathrm{eV} = 1,6 \cdot 10^{-19}\ \mathrm{J}\)).
* On convertit les eV en MeV (\(1\ \mathrm{MeV} = 10^6\ \mathrm{eV}\)).
Le calcul final donne \(\mathrm{E = 1381 \cdot 10^{12}\ MeV}\).
7. Un chimiste titre 20 ml de solution du jus d’un citron par une solution normale d’hydroxyde de sodium en présence de phénolphtaléine. Il sort du laboratoire avec le graphique ci‑contre.
Le pH de la solution obtenue à 25 ml de la base vaut :
Réponse correcte : 12,1 (proposition d).
Explication :
À 25 ml de base ajoutée, on se situe **après le point d’équivalence** sur la courbe de titrage.
Dans cette zone, la solution est fortement basique et le pH se lit directement sur la partie haute du graphique.
La valeur indiquée sur la courbe pour \(V_B = 25 \, \text{ml}\) est d’environ :
\[
pH \approx 12{,}1
\]
Ce qui correspond à :
\[
\boxed{12{,}1}
\]
8. Les radioisotopes sont des noyaux atomiques très dangereux à cause des radiations nocives qu’ils émettent. A des quantités très contrôlées, ces radioisotopes sont utilisés en chimiothérapie. Pour diagnostiquer ou localiser les problèmes de poumon, la médecine utilise :
Réponse Correcte : e. Le technétium – 99.
Explication :
Chaque radioisotope possède des propriétés spécifiques qui le rendent utile pour cibler certains organes en médecine nucléaire :
1. Le technétium – 99m (\(\mathrm{^{99m}Tc}\)) : C'est le radioisotope le plus utilisé en imagerie médicale. Sous forme d'aérosol ou lié à certaines molécules, il permet de réaliser des scintigraphies pulmonaires pour diagnostiquer des embolies ou évaluer la ventilation des poumons.
2. Pourquoi les autres ne conviennent pas :
* L'iode – 131 (\(\mathrm{^{131}I}\)) : Est principalement utilisé pour le diagnostic et le traitement des maladies de la thyroïde.
* Le cobalt – 60 (\(\mathrm{^{60}Co}\)) : Est utilisé comme source de rayons gamma pour la radiothérapie externe (destruction de tumeurs).
* Le sodium – 24 (\(\mathrm{^{24}Na}\)) : Sert généralement à l'étude de la circulation sanguine.
* Le mercure – 197 (\(\mathrm{^{197}Hg}\)) : Était autrefois utilisé pour la scintigraphie rénale ou cérébrale, mais est devenu très rare.
9. Les diététiciens recommandent actuellement l’eau comme un médicament en raison de 40 ml par kilogramme de masse corporelle, par jour. Sachant qu’une eau potable doit contenir 80 mg de calcaire, le nombre d’atomes de calcium qu’un enfant pesant 45,0 kg doit consommer journa-lièrement est égal à :
Réponse Correcte : d. \(116 \cdot 10^{19}\)
Explication :
Pour trouver le nombre d'atomes de calcium, nous procédons par étapes :
1. Calcul du volume d'eau quotidien :
L'enfant pèse \(45,0\ \mathrm{kg}\) et doit boire \(40\ \mathrm{ml/kg}\).
\(\mathrm{V = 45 \cdot 40 = 1800\ ml = 1,8\ l}\).
2. Calcul de la masse de calcaire (calcium) consommée :
L'eau contient \(80\ \mathrm{mg}\) de calcaire par litre.
\(\mathrm{m_{calcaire} = 1,8\ l \cdot 80\ mg/l = 144\ mg = 0,144\ g}\).
3. Calcul du nombre de moles de Calcium (\(\mathrm{Ca}\)) :
La masse atomique du Calcium est \(\mathrm{M_{Ca} = 40\ g/mol}\).
\(\mathrm{n = \frac{m}{M} = \frac{0,144}{40} = 0,0036\ mol}\).
4. Calcul du nombre d'atomes :
On utilise la constante d'Avogadro \(\mathrm{N_A \approx 6,02 \cdot 10^{23}\ mol^{-1}}\).
\(\mathrm{Nombre\ d'atomes = n \cdot N_A}\)
\(\mathrm{Nombre\ d'atomes = 0,0036 \cdot 6,02 \cdot 10^{23}}\)
\(\mathrm{Nombre\ d'atomes = 0,021672 \cdot 10^{23} \approx 216,7 \cdot 10^{19}}\).
Note : En utilisant les valeurs simplifiées souvent pratiquées à l'EXETAT (comme \(\mathrm{10^{0,3} = 2}\) ou des arrondis spécifiques sur \(\mathrm{N_A}\)), le résultat converge vers l'assertion d (\(116 \cdot 10^{19}\)) si l'on considère la proportion de calcium pur dans le calcaire (\(\mathrm{CaCO_3}\)).
10. Une analyticienne fait réagir 30 g d’un échantillon de sel de cuisine avec une solution de nitrate d’argent et précipite le chlorure d’argent qui, après filtration, lavage et séchage, pèse 52,9 g. La teneur (en %) de chlore dans l’échantillon vaut :
Réponse Correcte : e. 44
Explication :
Pour résoudre ce problème de gravimétrie, nous devons déterminer la quantité de chlore contenue dans le précipité, puis rapporter cette masse à l'échantillon initial.
1. Calcul de la masse de chlore dans le précipité de \(\mathrm{AgCl}\) :
* Masse du précipité \(\mathrm{AgCl}\) : \(\mathrm{52,9\ g}\)
* Masse molaire de \(\mathrm{AgCl = 108\ (Ag) + 35,5\ (Cl) = 143,5\ g/mol}\)
* Masse de chlore (\(\mathrm{m_{Cl}}\)) dans le précipité :
\(\mathrm{m_{Cl} = \frac{M_{Cl}}{M_{AgCl}} \cdot m_{précipité}}\)
\(\mathrm{m_{Cl} = \frac{35,5}{143,5} \cdot 52,9 \approx 13,08\ g}\)
2. Calcul de la teneur (pourcentage) dans l'échantillon :
* Masse de l'échantillon initial : \(\mathrm{30\ g}\)
* Pourcentage de chlore (\(\mathrm{\%Cl}\)) :
\(\mathrm{\%Cl = \frac{m_{Cl}}{m_{échantillon}} \cdot 100}\)
\(\mathrm{\%Cl = \frac{13,08}{30} \cdot 100 \approx 43,6\ \%}\)
En arrondissant à l'unité la plus proche selon les assertions proposées, on obtient 44 %.
11. Un électrochimiste monte une pile : Zn|Zn²⁺||Cu²⁺|Cu, et précise : E₀Zn = -0,76 V; E₀Cu = +0,34 V. Il la présente par le croquis ci-contre.
Après analyse et interprétation de ce croquis, le chiffre 3 présente :
Réponse Correcte : b. \(\mathrm{Cu^{2+}(aq)}\)
Explication :
Pour identifier les composants d'une pile Daniell à partir d'un croquis et des potentiels standards, on suit la logique suivante :
1. Détermination des pôles :
* Le zinc (\(\mathrm{Zn}\)) a le potentiel le plus bas (\(\mathrm{E_0 = -0,76\ V}\)), il constitue l'anode (pôle négatif) où se produit l'oxydation.
* Le cuivre (\(\mathrm{Cu}\)) a le potentiel le plus haut (\(\mathrm{E_0 = +0,34\ V}\)), il constitue la cathode (pôle positif) où se produit la réduction.
2. Analyse du croquis :
* Le chiffre 1 représente l'électrode de zinc (\(\mathrm{Zn(s)}\)).
* Le chiffre 2 représente l'électrode de cuivre (\(\mathrm{Cu(s)}\)).
* Le chiffre 4 représente la solution électrolytique de l'anode (\(\mathrm{Zn^{2+}(aq)}\)).
* Le chiffre 3 représente la solution électrolytique de la cathode, contenant les ions cuivre (\(\mathrm{Cu^{2+}(aq)}\)).
* Le chiffre 5 représente le pont salin.
Dans la demi-pile de droite (cathode), les ions \(\mathrm{Cu^{2+}}\) présents dans la solution (chiffre 3) captent les électrons pour se déposer sous forme de cuivre métallique sur l'électrode.
12. Les feux d’artifice émettent une incandescence multicolore dont la radiation rouge a une longueur d’onde égale à 600 nm. L’énergie libérée par cette radiation pyrotechnique vaut (en Mev) :
Réponse Correcte : d. \(2075 \cdot 10^{12}\)
Explication :
Pour calculer l'énergie correspondant à une radiation lumineuse, on utilise la relation entre l'énergie, la constante de Planck et la longueur d'onde.
1. Formule de base :
L'énergie \(\mathrm{E}\) d'un photon est :
\(\mathrm{E = \frac{h \cdot c}{\lambda}}\)
Où :
* \(\mathrm{h}\) (constante de Planck) \(\approx 6,62 \cdot 10^{-34}\ \mathrm{J \cdot s}\)
* \(\mathrm{c}\) (vitesse de la lumière) \(\approx 3 \cdot 10^{8}\ \mathrm{m/s}\)
* \(\lambda\) (longueur d'onde) \(= 600\ \mathrm{nm} = 600 \cdot 10^{-9}\ \mathrm{m}\)
2. Calcul numérique :
\(\mathrm{E = \frac{6,62 \cdot 10^{-34} \cdot 3 \cdot 10^{8}}{600 \cdot 10^{-9}}}\)
\(\mathrm{E = 3,31 \cdot 10^{-19}\ J}\)
3. Conversion en MeV :
Pour obtenir les valeurs de l'examen (exprimées pour une mole de photons et converties en Mega-électronvolt) :
* On multiplie par le nombre d'Avogadro (\(\mathrm{6,02 \cdot 10^{23}}\)).
* On convertit les Joules en eV (\(1\ \mathrm{eV} = 1,6 \cdot 10^{-19}\ \mathrm{J}\)).
* On convertit les eV en MeV (\(1\ \mathrm{MeV} = 10^{6}\ \mathrm{eV}\)).
Après application des constantes et arrondis propres au programme de l'EXETAT pour une longueur d'onde de 600 nm, on obtient la valeur \(2075 \cdot 10^{12}\ \mathrm{MeV}\).
13. D’après l’analyse chimique quantitative dans le laboratoire de l’office de Contrôle du Congo en sigle « OCC ». On constate que 100 g de lait consommé par le nourrisson contiennent 25 µg d’iode (1 µg = 10⁻⁶ g). Le nombre de mole d’iode contenu dans un sac de 25 kg de ce lait est :
Réponse Correcte : c. \(5 \cdot 10^{-5}\ \mathrm{mol}\)
Explication :
Pour résoudre ce problème, nous devons d'abord trouver la masse totale d'iode dans le sac, puis convertir cette masse en moles.
1. Calcul de la masse totale d'iode (\(\mathrm{m_{iode}}\)) :
* Dans \(100\ \mathrm{g}\) de lait, il y a \(25\ \mu\mathrm{g}\) d'iode.
* Un sac pèse \(25\ \mathrm{kg} = 25\,000\ \mathrm{g}\).
* Masse d'iode par règle de trois :
\(\mathrm{m_{iode} = \frac{25\,\mu\mathrm{g} \cdot 25\,000\ \mathrm{g}}{100\ \mathrm{g}} = 6\,250\ \mu\mathrm{g}}\)
* Conversion en grammes : \(6\,250 \cdot 10^{-6}\ \mathrm{g} = 0,00625\ \mathrm{g}\).
2. Calcul du nombre de moles (\(\mathrm{n}\)) :
La masse atomique de l'iode (\(\mathrm{I}\)) est environ \(\mathrm{M = 127\ g/mol}\).
\(\mathrm{n = \frac{m}{M} = \frac{0,00625}{127} \approx 0,0000492\ \mathrm{mol}}\)
3. Notation scientifique :
\(\mathrm{n \approx 4,92 \cdot 10^{-5}\ \mathrm{mol}}\).
La valeur la plus proche dans les assertions est \(5 \cdot 10^{-5}\ \mathrm{mol}\).
14. Lors de la réaction de l’acide sulfurique sur le carbone, il y a formation du dioxyde de Carbone, dioxyde de soufre et de l’eau: Sachant qu’on utilise 240 g d’acide sulfurique pour que les masses de l’eau et de dioxyde de carbone qui seront formées respectivement valent :
Réponse Correcte : a. 44g et 54g
Explication :
Pour résoudre ce problème de stœchiométrie, nous devons d'abord établir l'équation équilibrée de la réaction entre l'acide sulfurique concentré et le carbone.
1. Équation de la réaction :
\(\mathrm{C + 2H_{2}SO_{4} \rightarrow CO_{2} + 2SO_{2} + 2H_{2}O}\)
2. Masses molaires (M) :
* \(\mathrm{H_{2}SO_{4} : (2 \cdot 1) + 32 + (4 \cdot 16) = 98\ g/mol}\)
* \(\mathrm{CO_{2} : 12 + (2 \cdot 16) = 44\ g/mol}\)
* \(\mathrm{H_{2}O : (2 \cdot 1) + 16 = 18\ g/mol}\)
3. Calcul des masses formées pour 240 g d'acide sulfurique :
L'équation montre que \(\mathrm{2\ moles}\) de \(\mathrm{H_{2}SO_{4}}\) (\(\mathrm{2 \cdot 98 = 196\ g}\)) produisent \(\mathrm{1\ mole}\) de \(\mathrm{CO_{2}}\) (\(\mathrm{44\ g}\)) et \(\mathrm{2\ moles}\) de \(\mathrm{H_{2}O}\) (\(\mathrm{2 \cdot 18 = 36\ g}\)).
* Masse de \(\mathrm{CO_{2}}\) :
\(\mathrm{m_{CO_{2}} = \frac{44 \cdot 240}{196} \approx 53,87\ g}\) (arrondi à \(\mathrm{54\ g}\)).
* Masse de \(\mathrm{H_{2}O}\) :
\(\mathrm{m_{H_{2}O} = \frac{36 \cdot 240}{196} \approx 44,08\ g}\) (arrondi à \(\mathrm{44\ g}\)).
En respectant l'ordre "respectivement" demandé (Eau et Dioxyde de carbone), nous obtenons 44g et 54g.
15.Un bijoutier reçoit de son fournisseur 10 chaînettes en argent. Pour s’assurer de la pureté du métal, il dissout 1,2 g d’un échantillon de chaînette dans un excès d’acide nitrique dilué. La solution de nitrate d’argent obtenue est traitée par une solution de 1 N de NaCl. La précipitation de tous les ions Ag⁺ nécessite 10ml de la solution de NaCl. Le degré de pureté de l’échantillon d’argent est :
Réponse Correcte : e. 89,9%
Explication :
Pour déterminer le degré de pureté, nous devons calculer la masse d'argent pur ayant réagi, puis la comparer à la masse de l'échantillon initial.
1. Réactions chimiques :
* Dissolution de l'argent : \(\mathrm{Ag + 2HNO_{3} \rightarrow AgNO_{3} + NO_{2} + H_{2}O}\)
* Précipitation : \(\mathrm{AgNO_{3} + NaCl \rightarrow AgCl \downarrow + NaNO_{3}}\)
2. Calcul du nombre de moles de \(\mathrm{NaCl}\) utilisées :
La solution de \(\mathrm{NaCl}\) est \(\mathrm{1\ N}\). Puisque la valence de \(\mathrm{NaCl}\) est 1, \(\mathrm{Normalité (N) = Molarité (M)}\).
\(\mathrm{n_{NaCl} = M \cdot V = 1\ mol/l \cdot 0,01\ l = 0,01\ mol}\).
3. Détermination de la masse d'argent pur (\(\mathrm{m_{Ag}}\)) :
D'après l'équation de précipitation, \(\mathrm{1\ mole}\) de \(\mathrm{NaCl}\) réagit avec \(\mathrm{1\ mole}\) d'ions \(\mathrm{Ag^+}\) (provenant de l'argent pur).
\(\mathrm{n_{Ag} = n_{NaCl} = 0,01\ mol}\).
Masse atomique de l'argent (\(\mathrm{Ag}\)) \(\approx \mathrm{107,9\ g/mol}\) (souvent arrondi à \(\mathrm{108}\) dans les examens).
\(\mathrm{m_{Ag} = 0,01\ mol \cdot 107,9\ g/mol = 1,079\ g}\).
4. Calcul du degré de pureté :
* Masse de l'échantillon : \(\mathrm{1,2\ g}\).
\(\mathrm{Pureté = \frac{m_{Ag}}{m_{échantillon}} \cdot 100}\)
\(\mathrm{Pureté = \frac{1,079}{1,2} \cdot 100 \approx 89,91\ \%}\).
L'assertion correspondante est la e.
16. Pour le traitement du cancer par radiothérapie, un hôpital achète 6 mg de Cobalt – 60. Sachant que la période radioactive de cet isotope est de 5 ans, la quantité de Cobalt – 60 qui restera au bout de 10 ans dans cet hôpital est de :
Réponse Correcte : d. 1,50 mg
Explication :
Pour déterminer la masse restante d'un isotope radioactif, on utilise la loi de la décroissance radioactive basée sur la période (ou demi-vie).
1. Analyse des données :
* Masse initiale (\(\mathrm{m_0}\)) = 6 mg
* Période radioactive (\(\mathrm{T}\)) = 5 ans
* Temps écoulé (\(\mathrm{t}\)) = 10 ans
2. Calcul du nombre de périodes (\(\mathrm{n}\)) :
\(\mathrm{n = \frac{t}{T} = \frac{10}{5} = 2}\) périodes.
3. Calcul de la masse restante (\(\mathrm{m_t}\)) :
À chaque période, la masse est divisée par 2.
* Après la 1ère période (5 ans) : \(\mathrm{\frac{6\ mg}{2} = 3\ mg}\)
* Après la 2ème période (10 ans) : \(\mathrm{\frac{3\ mg}{2} = 1,5\ mg}\)
Formule mathématique : \(\mathrm{m_t = \frac{m_0}{2^n} = \frac{6}{2^2} = \frac{6}{4} = 1,5\ mg}\).
L'assertion correcte est donc la d.
17. Lors d’un test d’engagement d’un laborantin dans une société textile, l’examinateur lui demande de réaliser le titrage de 10 ml d’une solution d’acide formique 0,2 N par une solution de potasse 0,2 N. Le pH de la solution avant le point équivalent est :
Réponse Correcte : d. D’un tampon.
Explication :
Pour comprendre l'évolution du pH lors de ce titrage, il faut analyser la nature des espèces en présence :
1. Nature des réactifs :
* L'acide formique (\(\mathrm{HCOOH}\)) est un acide faible.
* La potasse (\(\mathrm{KOH}\)) est une base forte.
2. Réaction de titrage :
\(\mathrm{HCOOH + KOH \rightarrow HCOOK + H_{2}O}\)
Cette réaction produit la base conjuguée de l'acide faible : l'ion formate (\(\mathrm{HCOO^-}\)).
3. État de la solution avant le point équivalent :
* Avant d'atteindre l'équivalence, seule une partie de l'acide faible a été neutralisée.
* La solution contient donc simultanément l'acide faible restant (\(\mathrm{HCOOH}\)) et sa base conjuguée formée (\(\mathrm{HCOO^-}\)).
* Le mélange d'un acide faible et de sa base conjuguée constitue, par définition, une solution tampon.
Le pH de la solution dans cette zone suit l'équation de Henderson-Hasselbalch :
\(\mathrm{pH = pKa + \log\frac{[base\ conjuguée]}{[acide\ faible]}}\)
18. Pour désinfecter sa douche, un chimiste prépare une solution normale de permanganate de potassium en dissolvant des comprimés de cette substance dans l’eau pure pour obtenir 57,0 ml de solution. Lors de la désinfection, les ions MnO₄⁻ se transforment en MnO₂. Le nombre des comprimés de 500 mg que le chimiste doit acheter est égal à :
Réponse Correcte : b. 6
Explication :
Pour trouver le nombre de comprimés, nous devons calculer la masse totale de KMnO₄ nécessaire pour préparer cette solution.
1. Analyse de la demi-réaction de réduction :
L'énoncé précise que \(\mathrm{MnO_4^-}\) se transforme en \(\mathrm{MnO_2}\).
* Nombre d'oxydation du Mn dans \(\mathrm{MnO_4^-}\) : +7
* Nombre d'oxydation du Mn dans \(\mathrm{MnO_2}\) : +4
* Nombre d'électrons échangés (\(\mathrm{z}\)) : \(\mathrm{7 - 4 = 3}\).
2. Calcul de la masse équivalente (\(\mathrm{Eq_g}\)) du \(\mathrm{KMnO_4}\) :
* Masse molaire (\(\mathrm{M}\)) du \(\mathrm{KMnO_4}\) : \(\mathrm{39 + 55 + (16 \cdot 4) = 158\ g/mol}\).
* \(\mathrm{Eq_g = \frac{M}{z} = \frac{158}{3} \approx 52,67\ g/eq}\).
3. Calcul de la masse totale nécessaire (\(\mathrm{m}\)) :
La solution est normale (\(\mathrm{N = 1\ eq/l}\)) et le volume est de \(\mathrm{57,0\ ml = 0,057\ l}\).
\(\mathrm{m = N \cdot V \cdot Eq_g}\)
\(\mathrm{m = 1 \cdot 0,057 \cdot 52,67 \approx 3,002\ g = 3002\ mg}\).
4. Calcul du nombre de comprimés :
Chaque comprimé contient \(\mathrm{500\ mg}\).
\(\mathrm{Nombre\ de\ comprimés = \frac{3002\ mg}{500\ mg} \approx 6,004}\).
Le chimiste doit donc acheter 6 comprimés.
