Exetat de chimie de 2019-Scientifiques
1.La connaissance de la structure électronique des atomes et ions permet de justifier la formation des molécules, leurs propriétés et leurs structures spatiales. La structure électronique de la couche externe de l’argon est :
Correction accessible uniquement après paiement.
Payer pour voir la correction
2.L’électron de l’atome d’hydrogène situé au niveau \(n_1 = 1\), reçoit une lumière ultraviolette pour se retrouver au niveau \(n_2 = 5\). L’énergie de cette lumière ultraviolette est :
Correction accessible uniquement après paiement.
Payer pour voir la correction
3.Un médecin pratiquant la chimiothérapie place 0,012 g d’un radioélément de période 5 ans dans le corps d’un malade souffrant d’un cancer de sang. Les rayonnements libérés par le radioélément bombardent les cellules cancéreuses. A la guérison complète du malade, le médecin analyse et constate qu’il reste 0,003 g du radioélément. La durée de traitement du malade est de (en nombre d’années) :
Correction accessible uniquement après paiement.
Payer pour voir la correction
4.L’acétylène \(\text{C}_2\text{H}_2\), utilisé comme combustible, est préparé par action de carbure de calcium \(\text{CaC}_2\) sur l’eau. Quel volume d’acétylène (en L, CNTP) obtient-on à partir de \(120\ \text{g}\) de \(\text{CaC}_2\) ?
Correction accessible uniquement après paiement.
Payer pour voir la correction
5.Un réacteur nucléaire est un appareil capable de maitriser la fission d’un noyau et de canaliser l’énergie liberée vers les usages scientifiques, militaires, industriels ou domestiques. Indiquez les corps chimiques utilisables comme réfrigérant ou corps caloporteur dans un réacteur nucléaire.
Correction accessible uniquement après paiement.
Payer pour voir la correction
6.Un chimiste achète 100 g d’oxyde de fer rouge pour fabriquer 4 kg d’antirouille. Le nombre de boîtes de 2,5 Kg d’antirouille à fabriquer à partir de 0,625 Kg d’oxyde de fer rouge est de :
Correction accessible uniquement après paiement.
Payer pour voir la correction
7.De l’eau distillée exposée à l’atmosphère a un pH de \(5{,}4\). Quelle est la masse des ions \(\text{H}^+\) dans \(12\ \text{L}\) de cette eau ?
Correction accessible uniquement après paiement.
Payer pour voir la correction
8.L’acide benzoïque est un additif alimentaire utilisé comme agent de conservation des jus de fruits. Sa formule chimique est la suivante :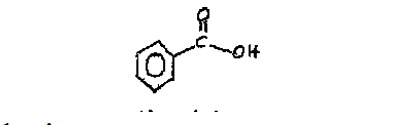
Cet acide existe dans le jus à une concentration centinormale. Le volume du jus de fruits contenant 0,1464 g d’acide benzoïque est de (en ml) :
Correction accessible uniquement après paiement.
Payer pour voir la correction
9.On dissout 2 g d’hydroxyde de sodium dans 185 ml de solution. Indiquez le pH.
Correction accessible uniquement après paiement.
Payer pour voir la correction
10.Un échantillon de calcaire de 1,92 g est dissous dans une solution de chlorure d’hydrogène. Le calcium, précipité par une solution d’oxalate d’ammonium en présence d’ammoniaque, est chauffé à près de 400 °C et transformé en carbonate de calcium 1,45 g. Indiquez le titre du calcium dans le calcaire.
Correction accessible uniquement après paiement.
Payer pour voir la correction
11.Indiquez les coefficients stœchiométriques de la réaction suivante : \[ \text{H}_2\text{SO}_3 + \text{I}_2 + \text{H}_2\text{O} \rightarrow \text{H}_2\text{SO}_4 + \text{HI} \]
Correction accessible uniquement après paiement.
Payer pour voir la correction
12.Indiquez la nomenclature du composé suivant : \[ \text{FeSO}_4 \cdot (\text{NH}_4)_2\text{SO}_4 \cdot 6\text{H}_2\text{O}\]
Correction accessible uniquement après paiement.
Payer pour voir la correction
13.Indiquez la molarité d’une solution de chlorure d’argent sachant que 83 ml de cette solution réagissent complètement avec une solution contenant 3,30 g de NaCl.
Correction accessible uniquement après paiement.
Payer pour voir la correction
14.Lors d’une oxydation par le permanganate de potassium en milieu acide, le pH influence le potentiel redox du système. Sachant qu’à pH = 0, \([\text{MnO}_4^-] = [\text{Mn}^{2+}]\), indiquez le potentiel redox à pH = 5.
Correction accessible uniquement après paiement.
Payer pour voir la correction
15.Indiquez la forme spatiale de la molécule de pentachlorure de phosphore :
Correction accessible uniquement après paiement.
Payer pour voir la correction
16.La radioactivité est un phénomène au cours du quel le noyau d’un atome se transmute en émettant des rayonnements. La particularité du rayonnement gamma est qu’il :
Correction accessible uniquement après paiement.
Payer pour voir la correction
17.Un agronome utilise une lampe UV projetant une lumière d’énergie \(E = 6{,}625 \cdot 10^{-19}\ \text{J}\). Quelle est la longueur d’onde associée ?
Correction accessible uniquement après paiement.
Payer pour voir la correction
18.Le bore absorbe les neutrons dans un réacteur nucléaire. Un échantillon contient : 10\% de \(^ {10}\text{B}\), 80\% de \(^ {14}\text{B}\), et une quantité de \(^ {15}\text{B}\). Quelle est la masse atomique moyenne du bore dans cet échantillon ?
Correction accessible uniquement après paiement.
Payer pour voir la correction
19.La transmutation permet à un atome de se transformer en un autre en émettant des radiations. Un atome de radon \((^{225}\text{Rn})\) se désintègre pour donner un atome d’astate \((^{221}\text{At})\). Quelles radiations sont libérées ?
Correction accessible uniquement après paiement.
Payer pour voir la correction
20.Un ajusteur utilisant le chalumeau oxyacétylénique pour souder les métaux achète 393g de gaz dioxygène contenu dans une bombonne de volume interne 25 litres, A 25°C, la pression à l’intérieur de la bombonne est de :
Correction accessible uniquement après paiement.
Payer pour voir la correction
21.La chloramphenicol est un antibiotique utilisé contre la fièvre typhoïde. Sa formule chimique est la suivante : 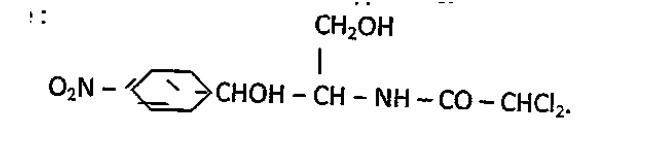
Un chimiste prépare une solution de chloramphénicol en dissolvant 1,615g de cet antibiotique dans l’eau jusqu’à obtenir 100 ml de solution.
La molarité de cette solution en chloramphénicol est de :
Correction accessible uniquement après paiement.
Payer pour voir la correction
22. Un environnementaliste puise l’eau usée provenant d’une usine de fabrication des batteries pour véhicules. Il constate après analyse que cette eau est acide et a un pH de 1,4 à cause de la présence de l’acide sulfurique. La molarité de cette eau usée en acide sulfirique est de :
Correction accessible uniquement après paiement.
Payer pour voir la correction
23. Un fabricant de savon obtient un carton de savon à partir de 3 kg d’hydroxyde de sodium. Le nombre de cartons de savon à obtenir à partir de 105 litres d’une solution d’hydroxyde de sodium 5N est de :
Correction accessible uniquement après paiement.
Payer pour voir la correction
24. Les indicateurs utilisés en volumétrie sont des substances capables de changer de coloration au point d’équivalence au cours d’un titrage. Indiquez la substance utilisée en bichromatométrie.
Correction accessible uniquement après paiement.
Payer pour voir la correction
25.L’eau oxygénée est un bactériostatique dont le pouvoir oxydant est donné par : \[ \text{H}_2\text{O}_2 + 2\text{H}^+ + 2e^- \rightarrow 2\text{H}_2\text{O} \quad E^\circ = 1{,}77\ \text{V} \] Quelle est le potentiel rédox à \(pH = 3\) et \([H_2O_2] = 0{,}01\ \text{mol/L}\) ?
Correction accessible uniquement après paiement.
Payer pour voir la correction
26.Un chimiste mélange 55 ml d’une solution de HCl 0,1 N avec une solution KOH 0,02 N. Le volume de la base au point d’équivalence est de :
Correction accessible uniquement après paiement.
Payer pour voir la correction
27.Les composés chimiques suivants : l’acide phosphorique, l’acide sulfureux, l’acide chlorique et l’acide sulfurique, présentent toutes les propriétés de la fonction acide. Ce sont des liquides dangereux et utilisés avec précaution. Indiquez la structure correcte pour l’acide sulfurique.
Correction accessible uniquement après paiement.
Payer pour voir la correction
28.Le bichromate est utilisé pour obtenir du KHSO\(_4\) par réaction redox : \[ \text{KClO}_3 + \text{H}_2\text{SO}_4 \rightarrow \text{KHSO}_4 + \text{O}_2 + \text{ClO}_2 + \text{H}_2\text{O} \] Indiquez les coefficients stœchiométriques de cette réaction :
Correction accessible uniquement après paiement.
Payer pour voir la correction
29.Un morceau d’acier au nickel de \(1{,}00\ \text{g}\) donne un précipité rouge de \(\text{Ni(C}_4\text{H}_7\text{O}_2\text{N}_2)_2\) pesant \(0{,}150\ \text{g}\). Quel est le pourcentage de nickel dans l’alliage ?
Correction accessible uniquement après paiement.
Payer pour voir la correction
30.Lors d’une réaction chimique, les réactifs entrent en collision efficace pour donner des corps nouveaux appelés : produits de la réaction. Indiquez l’équation qui représente une demi-équation de réduction
Correction accessible uniquement après paiement.
Payer pour voir la correction